انتقال آدیاباتیک بین دو حالت در گازها یکی از فرآیندهای همسان نیست، با این حال، نه تنها در فرآیندهای مختلف فناوری، بلکه در طبیعت نیز نقش مهمی ایفا می کند. در این مقاله، این فرآیند چیست و همچنین معادلات آدیاباتیک یک گاز ایده آل را ارائه خواهیم کرد.
گاز ایده آل به طور خلاصه
گاز ایده آل گازی است که هیچ برهمکنشی بین ذرات آن وجود نداشته باشد و اندازه آنها برابر با صفر باشد. البته در طبیعت، گازهای صد در صد ایده آل وجود ندارند، زیرا همگی از مولکول ها و اتم هایی با اندازه تشکیل شده اند که همیشه حداقل با کمک نیروهای واندروالس با یکدیگر تعامل دارند. با این وجود، مدل توصیف شده اغلب با دقت کافی برای حل مسائل عملی برای بسیاری از گازهای واقعی انجام می شود.
معادله اصلی یک گاز ایده آل قانون کلاپیرون- مندلیف است. به شکل زیر نوشته شده است:
PV=nRT.
این معادله یک تناسب مستقیم بین محصول ایجاد می کندفشار P روی حجم V و مقدار ماده n روی دمای مطلق T. مقدار R ثابت گاز است که نقش یک ضریب تناسب را ایفا می کند.
فرایند آدیاباتیک چیست؟
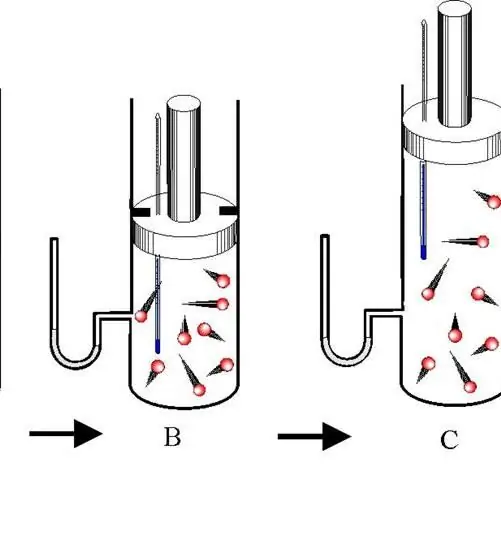
فرایند آدیاباتیک انتقالی بین حالت های یک سیستم گازی است که در آن تبادل انرژی با محیط وجود ندارد. در این حالت، هر سه مشخصه ترمودینامیکی سیستم (P، V، T) تغییر میکند و مقدار ماده n ثابت میماند.
بین انبساط و انقباض آدیاباتیک تمایز قائل شوید. هر دو فرآیند فقط به دلیل انرژی داخلی سیستم اتفاق می افتد. بنابراین در اثر انبساط، فشار و به خصوص دمای سیستم به شدت کاهش می یابد. برعکس، فشرده سازی آدیاباتیک منجر به جهش مثبت دما و فشار می شود.
برای جلوگیری از تبادل حرارت بین محیط و سیستم، سیستم دوم باید دارای دیوارهای عایق حرارتی باشد. علاوه بر این، کوتاه کردن زمان فرآیند به طور قابل توجهی جریان گرما را به سیستم و از سیستم کاهش می دهد.
معادلات پواسون برای یک فرآیند آدیاباتیک

قانون اول ترمودینامیک به صورت زیر نوشته شده است:
Q=ΔU + A.
به عبارت دیگر، گرمای Q ارسال شده به سیستم برای انجام کار A توسط سیستم و افزایش انرژی داخلی ΔU آن استفاده می شود. برای نوشتن معادله آدیاباتیک باید Q=0 قرار داد که با تعریف فرآیند مورد مطالعه مطابقت دارد. ما دریافت می کنیم:
ΔU=-A.
با ایزوکوریکفرآیند در یک گاز ایده آل، تمام گرما برای افزایش انرژی داخلی می رود. این واقعیت به ما اجازه می دهد تا برابری را بنویسیم:
ΔU=CVΔT.
که در آن CV ظرفیت گرمایی ایزوکوریک است. کار A به نوبه خود به صورت زیر محاسبه می شود:
A=PdV.
جایی که dV یک تغییر حجم کوچک است.
علاوه بر معادله کلاپیرون- مندلیف، معادله زیر برای گاز ایده آل صدق می کند:
CP- CV=R.
که در آن CP ظرفیت گرمایی همسان است، که همیشه از ظرفیت گرمایی ایزوباریک بیشتر است، زیرا تلفات گاز ناشی از انبساط را در نظر می گیرد.
با تجزیه و تحلیل معادلات نوشته شده در بالا و ادغام دما و حجم، به معادله آدیاباتیک زیر می رسیم:
TVγ-1=Const.
در اینجا γ شاخص آدیاباتیک است. برابر است با نسبت ظرفیت حرارتی ایزوباریک به ایزوکوریک. این برابری معادله پواسون برای یک فرآیند آدیاباتیک نامیده می شود. با استفاده از قانون Clapeyron-Mendeleev، می توانید دو عبارت مشابه دیگر را فقط از طریق پارامترهای P-T و P-V بنویسید:
TPγ/(γ-1)=const;
PVγ=Const.
گراف آدیاباتیک را می توان در محورهای مختلف ارائه داد. در زیر آن در محورهای P-V نشان داده شده است.
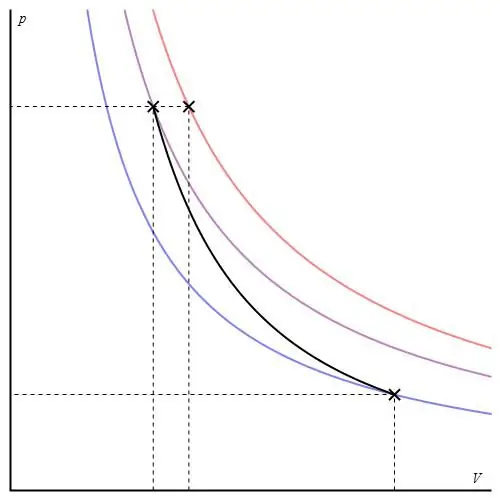
خطوط رنگی روی نمودار مربوط به همدما هستند، منحنی سیاه یک adiabat است. همانطور که مشاهده می شود، adiabat تندتر از هر یک از ایزوترم ها رفتار می کند. توضیح این واقعیت آسان است: برای ایزوترم، فشار دوباره تغییر می کندمتناسب با حجم است، اما برای ایزوبات، فشار سریعتر تغییر می کند، زیرا توان برای هر سیستم گازی γ>1 است.
مشکل مثال
در طبیعت، در مناطق کوهستانی، وقتی توده هوا از شیب بالا می رود، فشار آن کاهش می یابد، حجم آن افزایش می یابد و سرد می شود. این فرآیند آدیاباتیک نقطه شبنم را کاهش میدهد و بارش مایع و جامد ایجاد میکند.

برای حل مشکل زیر پیشنهاد می شود: در فرآیند بالا بردن توده هوا در امتداد شیب کوه، فشار 30٪ نسبت به فشار در پا کاهش یافت. اگر در پا 25 oC بود با چه دمایی برابر بود؟
برای حل مسئله، از معادله آدیاباتیک زیر استفاده کنید:
TPγ/(γ-1)=Const.
بهتر است به این شکل بنویسید:
T2/T1=(P2/P 1)(γ-1)/γ.
اگر P1 به عنوان 1 اتمسفر در نظر گرفته شود، P2 برابر با 0.7 اتمسفر خواهد بود. برای هوا، شاخص آدیاباتیک 1.4 است، زیرا می توان آن را یک گاز ایده آل دو اتمی در نظر گرفت. مقدار دمای T1 298.15 K است. با جایگزینی همه این اعداد در عبارت بالا، T2=269.26 K را دریافت می کنیم که مطابق با - 3، 9 oC.






