گاز ایده آل، معادله حالت گاز ایده آل، دما و فشار آن، حجم… فهرست پارامترها و تعاریف مورد استفاده در بخش مربوطه فیزیک را می توان برای مدت طولانی ادامه داد. امروز فقط در مورد این موضوع صحبت خواهیم کرد.
چه چیزی در فیزیک مولکولی در نظر گرفته می شود؟

جسم اصلی در نظر گرفته شده در این بخش یک گاز ایده آل است. معادله حالت گاز ایده آل با در نظر گرفتن شرایط طبیعی محیطی به دست آمده است و کمی بعد در مورد آن صحبت خواهیم کرد. حالا بیایید از دور به این "مشکل" نزدیک شویم.
فرض کنید مقداری گاز داریم. وضعیت آن را می توان با استفاده از سه پارامتر از طبیعت ترمودینامیکی تعیین کرد. اینها البته فشار، حجم و دما هستند. معادله وضعیت سیستم در این حالت فرمول رابطه بین پارامترهای مربوطه خواهد بود. به نظر می رسد: F (p، V، T)=0.
اینجا، برای اولین بار، کم کم داریم به ظهور چیزی به عنوان ایده آل نزدیک می شویم.گاز. گازی نامیده می شود که در آن برهمکنش بین مولکول ها ناچیز است. به طور کلی، این در طبیعت وجود ندارد. با این حال، هر گاز بسیار کمیاب به آن نزدیک است. نیتروژن، اکسیژن و هوا که در شرایط عادی قرار دارند، تفاوت کمی با حالت ایده آل دارند. برای نوشتن معادله حالت گاز ایده آل می توان از قانون گاز یکپارچه استفاده کرد. دریافت می کنیم: pV/T=const.
مفهوم مرتبط 1: قانون آووگادرو
او می تواند به ما بگوید که اگر به همان تعداد مول از هر گاز کاملاً تصادفی را برداریم و آنها را در شرایط یکسانی از جمله دما و فشار قرار دهیم، آنگاه گازها حجم یکسانی را اشغال خواهند کرد. به طور خاص، آزمایش در شرایط عادی انجام شد. این بدان معنی است که دما 273.15 کلوین، فشار یک اتمسفر (760 میلی متر جیوه یا 101325 پاسکال) بود. با این پارامترها، گاز حجمی معادل 22.4 لیتر را اشغال کرد. بنابراین، می توان گفت که برای یک مول از هر گاز، نسبت پارامترهای عددی یک مقدار ثابت خواهد بود. به همین دلیل تصمیم گرفته شد که این رقم را با حرف R تعیین کرده و آن را ثابت گاز جهانی نامیده شود. بنابراین، برابر 8.31 است. واحد J/molK است.
گاز ایده آل. معادله حالت گاز ایده آل و دستکاری آن
بیایید سعی کنیم فرمول را بازنویسی کنیم. برای این کار آن را به این شکل می نویسیم: pV=RT. بعد، یک عمل ساده انجام می دهیم، هر دو طرف معادله را در تعداد دلخواه مول ضرب می کنیم. ما pVu=uRT را دریافت می کنیم. اجازه دهید این واقعیت را در نظر بگیریم که حاصلضرب حجم مولی ومقدار ماده به سادگی حجم است. اما به هر حال، تعداد مول ها به طور همزمان برابر با ضریب جرم و جرم مولی خواهد بود. این دقیقاً همان چیزی است که معادله مندلیف-کلاپیرون به نظر می رسد. این ایده روشنی از نوع سیستمی که یک گاز ایده آل تشکیل می دهد به دست می دهد. معادله حالت یک گاز ایده آل به این شکل خواهد بود: pV=mRT/M.
استنتاج فرمول فشار
بیایید چند دستکاری بیشتر با عبارات به دست آمده انجام دهیم. برای انجام این کار، سمت راست معادله مندلیف-کلاپیرون ضرب و بر عدد آووگادرو تقسیم می شود. اکنون حاصل ضرب مقدار ماده را با عدد آووگادرو به دقت بررسی می کنیم. این چیزی نیست جز تعداد کل مولکول های موجود در گاز. اما در عین حال، نسبت ثابت گاز جهانی به عدد آووگادرو برابر با ثابت بولتزمن خواهد بود. بنابراین، فرمول های فشار را می توان به صورت زیر نوشت: p=NkT/V یا p=nkT. در اینجا نماد n غلظت ذره است.
فرایندهای گاز ایده آل
در فیزیک مولکولی چیزی به نام ایزوفرایندها وجود دارد. اینها فرآیندهای ترمودینامیکی هستند که در سیستم با یکی از پارامترهای ثابت انجام می شوند. در این حالت جرم ماده نیز باید ثابت بماند. بیایید به طور خاص به آنها نگاه کنیم. بنابراین، قوانین یک گاز ایده آل.
فشار ثابت می ماند
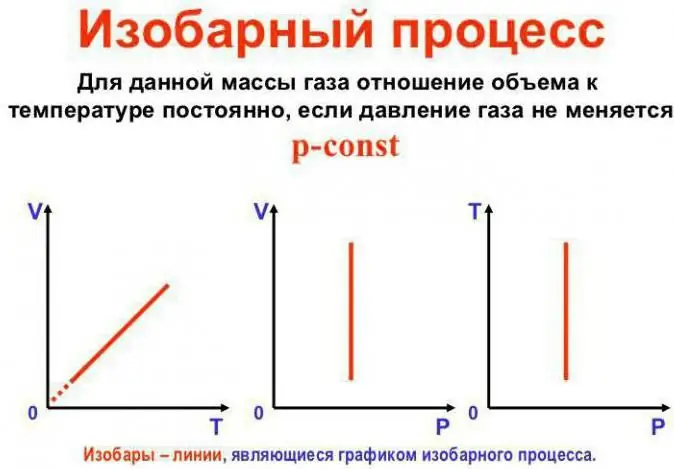
این قانون گی-لوساک است. به نظر می رسد این است: V/T=const. می توان آن را به روش دیگری بازنویسی کرد: V=Vo (1 + at). در اینجا a برابر با 1/273.15 K^-1 است و «ضریب انبساط حجمی» نامیده می شود. ما می توانیم دما را در هر دو درجه سانتیگراد ومقیاس کلوین در مورد دوم، فرمول V=Voat را دریافت می کنیم.
صدا ثابت می ماند

این دومین قانون گی-لوساک است که بیشتر به عنوان قانون چارلز شناخته می شود. به نظر می رسد این است: p/T=const. فرمول دیگری وجود دارد: p=po (1 + at). تغییرات را می توان مطابق با مثال قبلی انجام داد. همانطور که می بینید، قوانین گاز ایده آل گاهی کاملا شبیه یکدیگر هستند.
دما ثابت می ماند

اگر دمای یک گاز ایده آل ثابت بماند، می توانیم قانون بویل-ماریوت را بدست آوریم. می توان آن را اینگونه نوشت: pV=const.
مفهوم مرتبط 2: فشار جزئی
فرض کنید یک کشتی با گاز داریم. مخلوطی خواهد بود. سیستم در حالت تعادل حرارتی است و خود گازها با یکدیگر واکنش نشان نمی دهند. در اینجا N تعداد کل مولکول ها را نشان می دهد. N1، N2 و غیره، به ترتیب، تعداد مولکول ها در هر یک از اجزای مخلوط. اجازه دهید فرمول فشار p=nkT=NkT/V را در نظر بگیریم. می توان آن را برای یک مورد خاص باز کرد. برای مخلوط دو جزئی، فرمول به شکل p=(N1 + N2) kT/V خواهد بود. اما بعد معلوم می شود که فشار کل از فشارهای جزئی هر مخلوط جمع می شود. بنابراین، مانند p1 + p2 و غیره خواهد بود. اینها فشارهای جزئی خواهند بود.
برای چیست؟
فرمولی که به دست آوردیم نشان می دهد که فشار در سیستم از هر گروه از مولکول ها است. اتفاقاً به آن بستگی ندارددیگران. دالتون هنگام تدوین قانون که بعداً به نام او نامگذاری شد از این استفاده کرد: در مخلوطی که گازها از نظر شیمیایی با یکدیگر واکنش نمی دهند، فشار کل برابر با مجموع فشارهای جزئی خواهد بود.






