دنیایی که در آن زندگی می کنیم به طرز غیرقابل تصوری زیبا و پر از فرآیندهای مختلف است که مسیر زندگی را تعیین می کند. همه این فرآیندها توسط علم آشنا - فیزیک مورد مطالعه قرار می گیرند. این فرصتی را فراهم می کند تا حداقل ایده ای از منشاء جهان به دست آوریم. در این مقاله به مفهومی مانند نظریه جنبشی مولکولی، معادلات، انواع و فرمول های آن می پردازیم. با این حال، قبل از اینکه به مطالعه عمیقتری در مورد این مسائل بپردازید، باید خود معنای فیزیک و حوزههایی را که در آن مطالعه میکند، روشن کنید.
فیزیک چیست؟

در واقع، این علم بسیار گسترده و شاید یکی از اساسی ترین علوم در تاریخ بشریت است. به عنوان مثال، اگر همان علم کامپیوتر تقریباً با هر زمینه ای از فعالیت های انسانی مرتبط باشد، خواه طراحی محاسباتی باشد یا ایجاد کارتون، پس فیزیک خود زندگی است، توصیفی از فرآیندها و جریان های پیچیده آن. بیایید سعی کنیم معنی آن را بفهمیم و درک را تا حد امکان ساده کنیم.
پسبنابراین، فیزیک علمی است که با مطالعه انرژی و ماده، ارتباطات بین آنها، توضیح بسیاری از فرآیندهایی که در جهان وسیع ما رخ می دهند، سروکار دارد. نظریه مولکولی-سینتیکی ساختار ماده تنها یک قطره کوچک در دریای نظریه ها و شاخه های فیزیک است.
انرژی که این علم به تفصیل آن را مطالعه می کند، می تواند به اشکال مختلف نمایش داده شود. مثلاً به صورت نور، حرکت، گرانش، تشعشع، الکتریسیته و بسیاری اشکال دیگر. ما در این مقاله به نظریه جنبشی مولکولی ساختار این اشکال خواهیم پرداخت.
مطالعه ماده به ما ایده ای از ساختار اتمی ماده می دهد. به هر حال، از نظریه مولکولی-سینتیکی ناشی می شود. علم ساختار ماده به ما این امکان را می دهد که معنای وجود خود، دلایل پیدایش حیات و خود جهان را بفهمیم و پیدا کنیم. بیایید همچنان سعی کنیم نظریه جنبشی مولکولی ماده را مطالعه کنیم.
اول، مقدمه ای برای درک کامل اصطلاحات و هرگونه نتیجه گیری لازم است.
موضوعات فیزیک
در پاسخ به این سوال که نظریه مولکولی-سینتیک چیست، نمی توان در مورد بخش هایی از فیزیک صحبت نکرد. هر یک از اینها به مطالعه و توضیح دقیق حوزه خاصی از زندگی انسان می پردازد. آنها به شرح زیر طبقه بندی می شوند:
- مکانیک، که به دو بخش دیگر تقسیم می شود: سینماتیک و دینامیک.
- ایستا.
- ترمودینامیک.
- بخش مولکولی.
- الکترودینامیک.
- اپتیک.
- فیزیک کوانتوم ها و هسته اتم.
بیایید به طور خاص در مورد مولکولی صحبت کنیمفیزیک، زیرا بر اساس نظریه مولکولی جنبشی است.
ترمودینامیک چیست؟
به طور کلی، بخش مولکولی و ترمودینامیک شاخههای مرتبط نزدیکی از فیزیک هستند که منحصراً جزء ماکروسکوپی تعداد کل سیستمهای فیزیکی را مطالعه میکنند. شایان ذکر است که این علوم دقیقاً وضعیت درونی اجسام و مواد را توصیف می کنند. به عنوان مثال، حالت آنها در هنگام گرم شدن، تبلور، تبخیر و تراکم، در سطح اتمی. به عبارت دیگر، فیزیک مولکولی علم سیستم هایی است که از تعداد زیادی ذره تشکیل شده است: اتم ها و مولکول ها.
این علوم بودند که مفاد اصلی نظریه جنبشی مولکولی را مورد مطالعه قرار دادند.
حتی در کلاس هفتم با مفاهیم دنیای خرد و کلان، سیستم ها آشنا شدیم. تجدید این اصطلاحات در حافظه اضافی نخواهد بود.
جهان خرد، همانطور که از نام خود می بینیم، از ذرات بنیادی تشکیل شده است. به عبارت دیگر، اینجا دنیای ذرات کوچک است. اندازه آنها در محدوده 10-18 m تا 10-4 m اندازه گیری می شود، و زمان حالت واقعی آنها می تواند به بی نهایت و فواصل نامتناسب کوچک، برای مثال، 10-20 s.
Macroworld اجسام و سیستم هایی را با اشکال پایدار در نظر می گیرد که از ذرات بنیادی بسیاری تشکیل شده است. چنین سیستم هایی با اندازه انسان ما متناسب است.
علاوه بر این، چیزی به نام دنیای مگا وجود دارد. از سیارات عظیم، کهکشان ها و مجتمع های کیهانی تشکیل شده است.
اصولنظریه
اکنون که کمی خلاصه کردیم و اصطلاحات اصلی فیزیک را به خاطر آوردیم، می توانیم مستقیماً به موضوع اصلی این مقاله برویم.
نظریه مولکولی جنبشی ظاهر شد و برای اولین بار در قرن نوزدهم فرموله شد. ماهیت آن در این واقعیت نهفته است که ساختار هر ماده را با جزئیات توصیف می کند (اغلب ساختار گازها تا اجسام جامد و مایع)، بر اساس سه شرط اساسی که از مفروضات دانشمندان برجسته ای مانند رابرت هوک، آیزاک جمع آوری شده است. نیوتن، دانیل برنولی، میخائیل لومونوسوف و بسیاری دیگر.
مفاد اصلی نظریه جنبشی مولکولی به این صورت است:
- کاملاً همه مواد (صرف نظر از اینکه مایع، جامد یا گاز هستند) ساختار پیچیده ای دارند که از ذرات کوچکتر تشکیل شده است: مولکول ها و اتم ها. گاهی اوقات اتم ها را "مولکول های بنیادی" می نامند.
- همه این ذرات بنیادی همیشه در حالت حرکت مداوم و آشفته هستند. هر یک از ما به اثبات مستقیم این گزاره برخورد کرده ایم، اما، به احتمال زیاد، اهمیت زیادی برای آن قائل نشده ایم. به عنوان مثال، همه ما در پس زمینه پرتوهای خورشید دیدیم که ذرات گرد و غبار دائماً در یک جهت آشفته حرکت می کنند. این به دلیل این واقعیت است که اتم ها با یکدیگر فشارهای متقابل ایجاد می کنند و دائماً انرژی جنبشی را به یکدیگر منتقل می کنند. این پدیده برای اولین بار در سال 1827 مورد مطالعه قرار گرفت و به نام کاشف - "حرکت براونی" نامگذاری شد.
- همه ذرات بنیادی در فرآیند برهمکنش پیوسته با یکدیگر هستند.نیروهای خاصی که دارای سنگ الکتریکی هستند.
شایان ذکر است که مثال دیگری که موقعیت شماره دو را توصیف می کند، که ممکن است برای مثال در نظریه جنبشی مولکولی گازها نیز کاربرد داشته باشد، انتشار است. ما در زندگی روزمره و در آزمایشها و کنترلهای متعدد با آن مواجه میشویم، بنابراین داشتن ایده در مورد آن مهم است.
ابتدا به مثال های زیر توجه کنید:
دکتر به طور تصادفی الکل را از فلاسک روی میز ریخت. یا شاید بطری عطر خود را انداخته اید و روی زمین پخش شده است.
چرا در این دو مورد هم بوی الکل و هم بوی عطر بعد از مدتی کل اتاق را پر می کند و نه فقط قسمتی که محتویات این مواد ریخته شده است؟
پاسخ ساده است: انتشار.
انتشار - چیست؟ چگونه جریان دارد؟

این فرآیندی است که در آن ذراتی که یک ماده خاص (معمولاً گاز) را می سازند به داخل حفره های بین مولکولی ماده دیگر نفوذ می کنند. در مثالهای بالا، موارد زیر اتفاق افتاد: به دلیل حرکت حرارتی، یعنی حرکت مداوم و تفکیکشده، مولکولهای الکل و/یا عطر در شکافهای بین مولکولهای هوا افتادند. به تدریج، تحت تأثیر برخورد با اتم ها و مولکول های هوا، در اطراف اتاق پخش می شوند. به هر حال، شدت انتشار، یعنی سرعت جریان آن، به چگالی مواد درگیر در انتشار و همچنین به انرژی حرکت اتم ها و مولکول های آنها بستگی دارد که جنبشی نامیده می شود. هر چه انرژی جنبشی بیشتر باشد، به ترتیب سرعت و شدت این مولکولها بیشتر میشود.
سریعترین فرآیند انتشار را می توان انتشار در گازها نامید. این به دلیل این واقعیت است که گاز از نظر ترکیبی همگن نیست، به این معنی که حفره های بین مولکولی در گازها به ترتیب فضای قابل توجهی را اشغال می کنند و فرآیند ورود اتم ها و مولکول های یک ماده خارجی به آنها آسان تر و سریع تر انجام می شود..
این فرآیند در مایعات کمی کندتر است. حل کردن حبه های شکر در یک فنجان چای تنها نمونه ای از انتشار یک جامد در مایع است.
اما طولانی ترین زمان انتشار در اجسامی با ساختار بلوری جامد است. این دقیقاً چنین است، زیرا ساختار جامدات همگن است و دارای یک شبکه بلوری قوی است که در سلول های آن اتم های جامد به ارتعاش در می آیند. به عنوان مثال، اگر سطوح دو میله فلزی به خوبی تمیز شوند و سپس با یکدیگر تماس پیدا کنند، پس از مدت زمان کافی می توانیم قطعات یک فلز را در فلز دیگر تشخیص دهیم و بالعکس.
مثل هر بخش اساسی دیگر، نظریه پایه فیزیک به بخش های جداگانه تقسیم می شود: طبقه بندی، انواع، فرمول ها، معادلات و غیره. بنابراین، ما اصول نظریه جنبشی مولکولی را یاد گرفتیم. این بدان معنی است که می توانید با خیال راحت به بررسی بلوک های نظری فردی ادامه دهید.
نظریه مولکولی جنبشی گازها
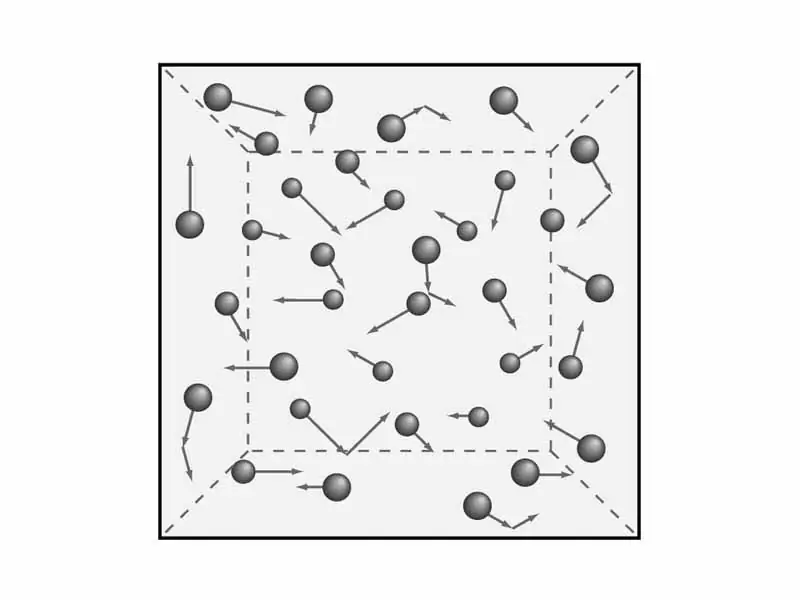
نیاز به درک مفاد تئوری گاز وجود دارد. همانطور که قبلاً گفتیم، ویژگی های ماکروسکوپی گازها مانند فشار و دما را در نظر خواهیم گرفت. این هستبعداً برای بدست آوردن معادله نظریه مولکولی-سینتیکی گازها مورد نیاز خواهد بود. اما ریاضیات - بعداً، و حالا بیایید به نظریه و بر این اساس، فیزیک بپردازیم.
دانشمندان پنج ماده از نظریه مولکولی گازها را فرموله کرده اند که برای درک مدل جنبشی گازها مفید است. صدای آنها اینگونه است:
- همه گازها از ذرات بنیادی تشکیل شده اند که اندازه مشخصی ندارند، اما جرم خاصی دارند. به عبارت دیگر، حجم این ذرات در مقایسه با طول بین آنها حداقل است.
- اتم ها و مولکول های گازها عملاً انرژی پتانسیل ندارند، طبق قانون، تمام انرژی برابر با جنبشی است.
- ما قبلاً با این موقعیت آشنا شدیم - حرکت براونی. یعنی ذرات گاز همیشه در حرکت پیوسته و آشفته هستند.
- کاملاً همه برخوردهای متقابل ذرات گاز، همراه با پیام سرعت و انرژی، کاملاً کشسان هستند. این به این معنی است که انرژی جنبشی آنها در هنگام برخورد از دست نمیرود یا پرش شدیدی ندارد.
- در شرایط عادی و دمای ثابت، میانگین انرژی حرکت ذرات تقریباً همه گازها یکسان است.
میتوانیم موقعیت پنجم را از طریق این نوع معادله نظریه مولکولی جنبشی گازها بازنویسی کنیم:
E=1/2mv^2=3/2kT،
که در آن k ثابت بولتزمن است. T - دما بر حسب کلوین.
این معادله به ما کمک می کند تا رابطه بین سرعت ذرات بنیادی گاز و دمای مطلق آنها را درک کنیم. بر این اساس، مطلق آنها بالاتر استدما، سرعت و انرژی جنبشی آنها بیشتر است.
فشار گاز
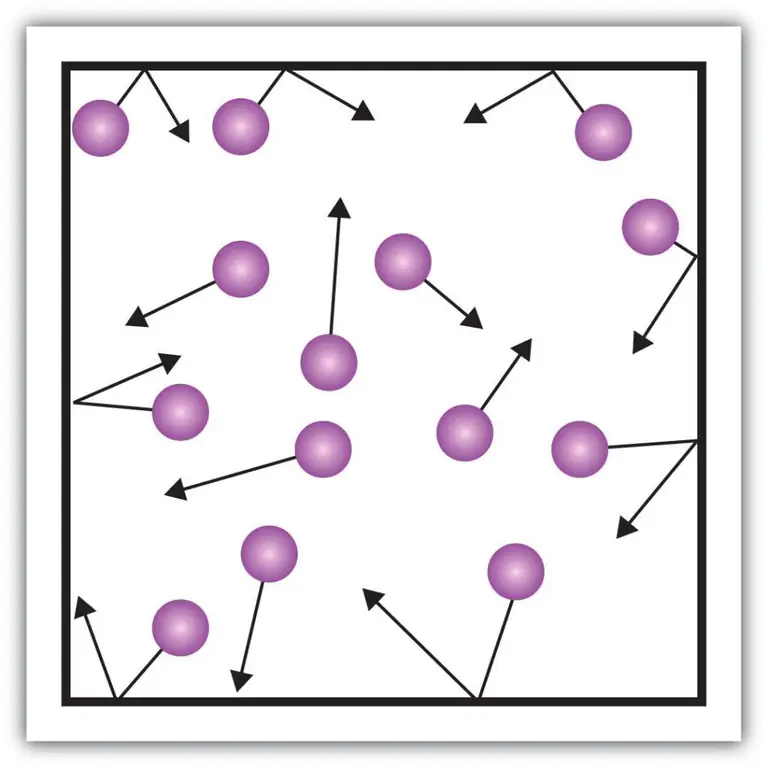
چنین مولفههای ماکروسکوپی مشخصه، مانند فشار گازها، را میتوان با استفاده از نظریه جنبشی توضیح داد. برای انجام این کار، بیایید مثال زیر را تصور کنیم.
فرض کنیم که یک مولکول گاز در جعبه ای است که طول آن L است. بیایید از مفاد نظریه گازی که در بالا توضیح داده شد استفاده کنیم و این واقعیت را در نظر بگیریم که کره مولکولی فقط در امتداد x حرکت می کند. -محور. بنابراین، ما قادر خواهیم بود روند برخورد الاستیک با یکی از دیواره های کشتی (جعبه) را مشاهده کنیم.
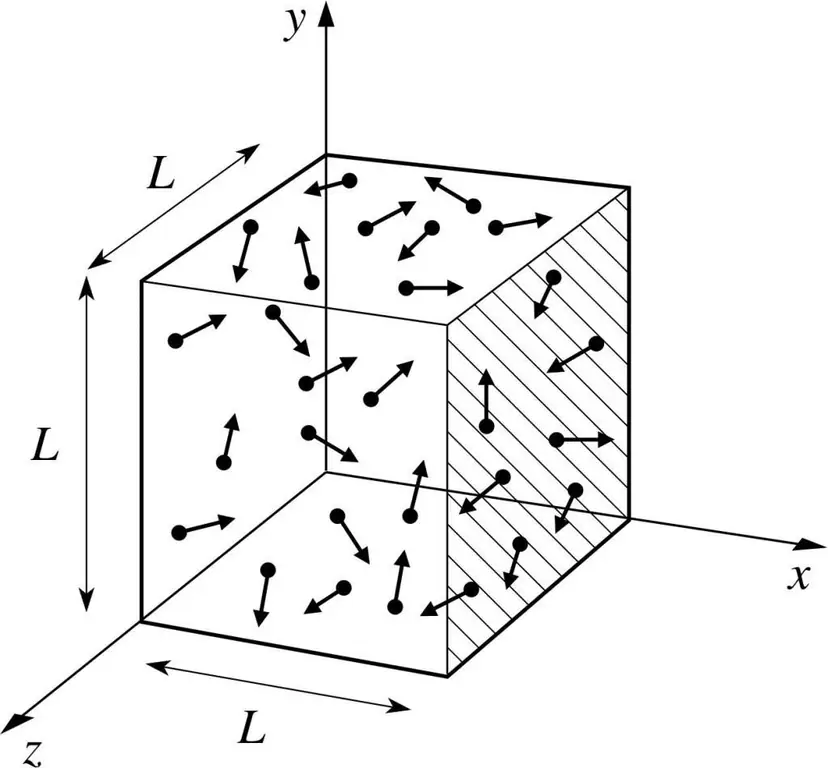
همانطور که می دانیم، تکانه برخورد در حال انجام با فرمول p=mv تعیین می شود، اما در این حالت، این فرمول به صورت طرح ریزی به خود می گیرد: p=mv(x).
از آنجایی که ما فقط بعد محور x، یعنی محور x را در نظر می گیریم، کل تغییر تکانه با فرمول بیان می شود: mv(x) - m(-v(x))=2mv(x).
بعد، نیروی اعمال شده توسط جسم ما را با استفاده از قانون دوم نیوتن در نظر بگیرید: F=ma=P/t.
از این فرمول ها فشار سمت گاز را بیان می کنیم: P=F/a;
حالا بیایید عبارت نیرو را در فرمول به دست آمده جایگزین کنیم و دریافت کنیم: P=mv(x)^2/L^3.
پس از آن، فرمول فشار نهایی ما را می توان برای N-امین تعداد مولکول های گاز نوشت. به عبارت دیگر، به این شکل خواهد بود:
P=Nmv(x)^2/V، که در آن v سرعت و V حجم است.
اکنون بیایید سعی کنیم چند شرط اساسی در مورد فشار گاز را برجسته کنیم:
- خود را از طریق نشان می دهدبرخورد مولکول ها با مولکول های دیواره جسمی که در آن قرار دارد.
- میزان فشار به طور مستقیم با نیرو و سرعت برخورد مولکول ها بر دیواره رگ نسبت دارد.
برخی نتیجه گیری کوتاه در مورد نظریه
قبل از اینکه فراتر برویم و معادله اصلی نظریه جنبشی مولکولی را در نظر بگیریم، چند نتیجه گیری کوتاه از نکات و نظریه فوق به شما ارائه می کنیم:
- معیار میانگین انرژی حرکت اتم ها و مولکول های آن دمای مطلق است.
- وقتی دو گاز مختلف در یک دما هستند، مولکول های آنها انرژی جنبشی متوسط یکسانی دارند.
- انرژی ذرات گاز با میانگین سرعت مربع نسبت مستقیم دارد: E=1/2mv^2.
- اگرچه مولکول های گاز به ترتیب دارای انرژی جنبشی متوسط و سرعت متوسط هستند، اما تک تک ذرات با سرعت های متفاوتی حرکت می کنند: برخی سریع، برخی آهسته.
- هر چه دما بالاتر باشد، سرعت مولکول ها بیشتر می شود.
- چند بار دمای گاز را افزایش می دهیم (مثلاً دو برابر)، انرژی حرکت ذرات آن چند برابر می شود (به ترتیب دو برابر می شود).
معادله و فرمول های اساسی

معادله اساسی نظریه جنبشی مولکولی به شما امکان می دهد تا رابطه بین کمیت های جهان خرد و بر این اساس، ماکروسکوپی، یعنی کمیت های اندازه گیری شده را برقرار کنید.
یکی از سادهترین مدلهایی که تئوری مولکولی میتواند در نظر بگیرد، مدل گاز ایدهآل است.
می توانید این را بگوییداین یک نوع مدل خیالی است که توسط نظریه جنبشی مولکولی یک گاز ایده آل مورد مطالعه قرار گرفته است که در آن:
- ساده ترین ذرات گاز به عنوان توپ های کاملاً الاستیک در نظر گرفته می شوند که هم با یکدیگر و هم با مولکول های دیواره هر ظرف تنها در یک مورد برهم کنش دارند - یک برخورد کاملاً الاستیک؛
- نیروهای جاذبه در داخل گاز وجود ندارند، یا در واقع می توان آنها را نادیده گرفت؛
- عناصر ساختار داخلی گاز را می توان به عنوان نقاط مادی در نظر گرفت، یعنی می توان حجم آنها را نیز نادیده گرفت.
با در نظر گرفتن چنین مدلی، فیزیکدان آلمانی الاصل رودولف کلازیوس فرمولی برای فشار گاز از طریق رابطه پارامترهای میکرو و ماکروسکوپی نوشت. به نظر می رسد:
p=1/3m(0)nv^2.
بعداً این فرمول به عنوان معادله پایه نظریه مولکولی- جنبشی یک گاز ایده آل نامیده می شود. می توان آن را در چندین شکل مختلف ارائه کرد. اکنون وظیفه ما نشان دادن بخش هایی مانند فیزیک مولکولی، نظریه جنبشی مولکولی و از این رو معادلات و انواع کامل آنهاست. بنابراین، منطقی است که سایر تغییرات فرمول اصلی را در نظر بگیریم.
می دانیم که میانگین انرژی مشخص کننده حرکت مولکول های گاز را می توان با استفاده از فرمول یافت: E=m(0)v^2/2.
در این مورد، می توانیم عبارت m(0)v^2 را در فرمول فشار اولیه با انرژی جنبشی متوسط جایگزین کنیم. در نتیجه این فرصت را خواهیم داشت تا معادله پایه نظریه جنبشی مولکولی گازها را به شکل زیر بسازیم: p=2/3nE.
علاوه بر این، همه ما می دانیم که عبارت m(0)n را می توان به صورت حاصل ضرب دو ضریب نوشت:
m/NN/V=m/V=ρ.
پس از این دستکاریها، میتوانیم فرمول خود را برای معادله نظریه مولکولی-سینتیکی یک گاز ایدهآل به شکل سوم و متفاوت بازنویسی کنیم:
p=1/3ρv^2.
خب، شاید این تنها چیزی است که باید در مورد این موضوع بدانید. تنها به نظام مند کردن دانش به دست آمده در قالب نتیجه گیری های مختصر (و نه چندان زیاد) باقی می ماند.
همه نتیجه گیری ها و فرمول های کلی در مورد موضوع "نظریه مولکولی-سینتیک"
پس بیایید شروع کنیم.
اول:
فیزیک یک علم بنیادی است که در درس علوم طبیعی گنجانده شده است و به بررسی خواص ماده و انرژی، ساختار آنها، الگوهای طبیعت معدنی می پردازد.
شامل بخشهای زیر است:
- مکانیک (سینماتیک و دینامیک)؛
- ایستا;
- ترمودینامیک;
- الکترودینامیک;
- بخش مولکولی;
- اپتیک;
- فیزیک کوانتوم ها و هسته اتم.
دومین:
فیزیک ذرات و ترمودینامیک شاخههای نزدیک به هم هستند که جزء منحصراً ماکروسکوپیک تعداد کل سیستمهای فیزیکی را مطالعه میکنند، یعنی سیستمهایی که از تعداد زیادی ذرات بنیادی تشکیل شدهاند.
آنها بر اساس نظریه جنبشی مولکولی هستند.
سوم:
اصل موضوع این است. تئوری جنبشی مولکولی ساختار یک ماده را به تفصیل توصیف می کند (اغلب ساختار گازها تا جامدات).و اجسام مایع) بر اساس سه فرض اساسی که از مفروضات دانشمندان برجسته جمع آوری شده است. از جمله: رابرت هوک، آیزاک نیوتن، دانیل برنولی، میخائیل لومونوسوف و بسیاری دیگر.
چهارم:
سه اصل اساسی نظریه جنبشی مولکولی:
- همه مواد (صرف نظر از اینکه مایع، جامد یا گاز هستند) ساختار پیچیده ای دارند که از ذرات کوچکتر تشکیل شده است: مولکول ها و اتم ها.
- همه این ذرات ساده در حرکت آشفته پیوسته هستند. مثال: حرکت و انتشار براونی.
- همه مولکول ها تحت هر شرایطی با نیروهای خاصی که دارای سنگ الکتریکی هستند با یکدیگر برهمکنش می کنند.
هر یک از این مفاد نظریه جنبشی مولکولی یک پایه محکم در مطالعه ساختار ماده است.
پنجم:
چند نکته اصلی نظریه مولکولی برای مدل گاز:
- همه گازها از ذرات بنیادی تشکیل شده اند که اندازه مشخصی ندارند، اما جرم خاصی دارند. به عبارت دیگر، حجم این ذرات در مقایسه با فواصل بین آنها حداقل است.
- اتم ها و مولکول های گازها به ترتیب عملاً انرژی پتانسیل ندارند، انرژی کل آنها برابر با انرژی جنبشی است.
- ما قبلاً با این موقعیت آشنا شدیم - حرکت براونی. یعنی ذرات گاز همیشه در حرکت پیوسته و تصادفی هستند.
- کاملاً تمام برخوردهای متقابل اتم ها و مولکول های گازها که با پیام سرعت و انرژی همراه است کاملاً کشسان هستند. این هستبه این معنی است که هیچ افت انرژی یا پرش شدیدی در انرژی جنبشی آنها در طول یک برخورد وجود ندارد.
- در شرایط عادی و دمای ثابت، میانگین انرژی جنبشی تقریباً همه گازها یکسان است.
ششم:
نتیجه گیری از نظریه گازها:
- دمای مطلق اندازه گیری میانگین انرژی جنبشی اتم ها و مولکول های آن است.
- وقتی دو گاز مختلف در یک دما هستند، مولکول های آنها انرژی جنبشی متوسط یکسانی دارند.
- میانگین انرژی جنبشی ذرات گاز با ریشه میانگین سرعت مربع رابطه مستقیم دارد: E=1/2mv^2.
- اگرچه مولکول های گاز به ترتیب دارای انرژی جنبشی متوسط و سرعت متوسط هستند، اما تک تک ذرات با سرعت های متفاوتی حرکت می کنند: برخی سریع، برخی آهسته.
- هر چه دما بالاتر باشد، سرعت مولکول ها بیشتر می شود.
- چند بار دمای گاز را افزایش می دهیم (مثلاً دو برابر)، میانگین انرژی جنبشی ذرات آن نیز چندین برابر (به ترتیب دو برابر) افزایش می یابد.
- رابطه بین فشار گاز بر روی دیوارههای ظرفی که در آن قرار دارد و شدت برخورد مولکولها بر این دیوارهها نسبت مستقیم دارد: هر چه ضربه بیشتر باشد، فشار بیشتر میشود و بالعکس..
هفتم:
یک مدل گاز ایده آل مدلی است که در آن شرایط زیر باید رعایت شود:
- مولکول های گاز می توانند و به عنوان توپ های کاملاً الاستیک در نظر گرفته شوند.
- این توپ ها می توانند با یکدیگر و با دیواره های هر کدام تعامل داشته باشندکشتی تنها در یک مورد - برخورد کاملاً الاستیک.
- آن نیروهایی که نیروی رانش متقابل بین اتمها و مولکولهای گاز را توصیف میکنند وجود ندارند یا در واقع میتوان آنها را نادیده گرفت.
- اتم ها و مولکول ها به عنوان نقاط مادی در نظر گرفته می شوند، یعنی می توان حجم آنها را نیز نادیده گرفت.
هشتم:
بیایید همه معادلات اساسی را ارائه دهیم و فرمول های موضوع "نظریه مولکولی- جنبشی" را نشان دهیم:
p=1/3m(0)nv^2 - معادله پایه برای مدل گاز ایده آل، که توسط فیزیکدان آلمانی رودولف کلازیوس مشتق شده است.
p=2/3nE - معادله اساسی نظریه مولکولی-سینتیکی یک گاز ایده آل. از میانگین انرژی جنبشی مولکول ها به دست می آید.
р=1/3ρv^2 - معادله یکسان، اما از طریق چگالی و ریشه میانگین سرعت مربع مولکولهای گاز ایدهآل در نظر گرفته میشود.
m(0)=M/N(a) - فرمول یافتن جرم یک مولکول از طریق عدد آووگادرو.
v^2=(v(1)+v(2)+v(3)+…)/N - فرمول برای یافتن میانگین سرعت مربع مولکول ها، که در آن v(1)، v(2) ، v (3) و غیره - سرعت مولکول اول، دوم، سوم و غیره تا مولکول n.
n=N/V - فرمول برای یافتن غلظت مولکول ها، که در آن N تعداد مولکول های یک حجم گاز به حجم معین V است.
E=mv^2/2=3/2kT - فرمولهایی برای یافتن انرژی جنبشی متوسط مولکولها، که در آن v^2 ریشه میانگین سرعت مربع مولکولها است، k یک ثابت است. مقدار به نام فیزیک اتریشی لودویگ بولتزمن نامگذاری شده است و T دمای گاز است.
p=nkT - فرمول فشار از نظر غلظت، ثابتبولتزمن و دمای مطلق T. از آن فرمول اساسی دیگری که توسط مندلیف دانشمند روسی و کلایپرون فیزیکدان-مهندس فرانسوی کشف شده است، پیروی می کند:
pV=m/MRT، که در آن R=kN(a) ثابت جهانی برای گازها است.
حالا بیایید ثابت هایی را برای فرآیندهای همسان مختلف نشان دهیم: ایزوباریک، ایزوکوریک، همدما و آدیاباتیک.
pV/T=const - زمانی انجام می شود که جرم و ترکیب گاز ثابت باشد.
рV=const - اگر دما نیز ثابت باشد.
V/T=const - اگر فشار گاز ثابت باشد.
p/T=const - اگر حجم ثابت باشد.
شاید این تنها چیزی است که باید در مورد این موضوع بدانید.
امروز ما وارد حوزه علمی مانند فیزیک نظری، بخش ها و بلوک های متعدد آن شدیم. با جزئیات بیشتر، ما به حوزه ای از فیزیک مانند فیزیک مولکولی بنیادی و ترمودینامیک، یعنی نظریه مولکولی جنبشی اشاره کردیم، که به نظر می رسد در مطالعه اولیه هیچ مشکلی ایجاد نمی کند، اما در واقع دارای مشکلات زیادی است.. این درک ما را از مدل گاز ایده آل، که ما نیز به طور مفصل مطالعه کردیم، گسترش می دهد. علاوه بر این، شایان ذکر است که ما همچنین با معادلات اساسی نظریه مولکولی در تغییرات مختلف آنها آشنا شدیم و همچنین تمام فرمول های ضروری برای یافتن مقادیر مجهول معین در این موضوع را در نظر گرفتیم که این امر به ویژه هنگام آماده شدن برای نوشتن مفید خواهد بود. هر گونه تست، امتحان و تست، یا برای گسترش دیدگاه و دانش عمومی فیزیک.
امیدواریم این مقاله برای شما مفید بوده باشد و تنها ضروری ترین اطلاعات را از آن استخراج کرده باشید و دانش خود را در زمینه ارکان ترمودینامیک به عنوان مفاد پایه نظریه جنبشی مولکولی تقویت کرده باشید.






