روش آنالیز هدایت سنجی اندازه گیری هدایت الکترولیتی برای نظارت بر پیشرفت یک واکنش شیمیایی است. این علم به طور گسترده در شیمی تجزیه استفاده می شود، جایی که تیتراسیون یک روش استاندارد عملیات است. هدایت سنجی چیست؟ در عمل رایج در شیمی تجزیه، این اصطلاح به عنوان مترادف برای تیتراسیون استفاده می شود، در حالی که برای توصیف کاربردهای غیر تیتراسیون نیز استفاده می شود. استفاده از این روش تحلیل چه فایده ای دارد؟ اغلب برای تعیین رسانایی کلی یک محلول یا برای تجزیه و تحلیل نقطه پایانی تیتراسیون شامل یون ها استفاده می شود.
تاریخ
اندازهگیریهای رسانا از اوایل قرن هجدهم شروع شد، زمانی که آندریاس بامگارتنر متوجه شد که نمک و آبهای معدنی از Bad Gastein دراتریش رسانای برق است. بنابراین، استفاده از این روش برای تعیین درجه خلوص آب که امروزه اغلب برای آزمایش اثربخشی سیستم های تصفیه آب استفاده می شود، از سال 1776 آغاز شد. بدین ترتیب تاریخچه روش هدایت سنجی تحلیل آغاز شد.
Friedrich Kohlrausch توسعه این علم را در دهه 1860 ادامه داد، زمانی که او جریان متناوب را به آب، اسیدها و محلول های دیگر اعمال کرد. در حوالی این زمان، ویلیس ویتنی که در حال مطالعه برهمکنشهای کمپلکسهای اسید سولفوریک و سولفات کروم بود، اولین نقطه پایانی هدایت سنجی را پیدا کرد. این یافته ها در تیتراسیون پتانسیومتری و اولین ابزار برای آنالیز حجمی توسط رابرت بهند در سال 1883 در تیتراسیون کلرید و برمید HgNO3 به اوج خود رسید. بنابراین، روش رسانایی مدرن تحلیل بر اساس Behrend است.
این پیشرفت آزمایش حلالیت نمک ها و غلظت یون های هیدروژن و همچنین تیتراسیون اسید-باز و ردوکس را ممکن کرد. روش آنالیز هدایت سنجی با توسعه الکترود شیشه ای که در سال 1909 آغاز شد، بهبود یافت.
تیتراژ
تیتراسیون هدایت سنجی اندازه گیری است که در آن هدایت الکترولیتی مخلوط واکنش به طور مداوم با افزودن یک معرف کنترل می شود. نقطه هم ارزی نقطه ای است که در آن رسانایی به طور ناگهانی تغییر می کند. افزایش یا کاهش قابل توجه در رسانایی با تغییر در غلظت دو یون بسیار رسانا، یون هیدروژن و هیدروکسید همراه است. این روشمی توان برای تیتراسیون محلول های رنگی یا سوسپانسیون همگن (مثلاً سوسپانسیون خمیر چوب) که با شاخص های معمولی قابل استفاده نیست استفاده کرد.
تیتراسیون اسید-باز و ردوکس اغلب انجام می شود که از شاخص های رایج برای تعیین نقطه پایانی استفاده می کند، مانند متیل اورانژ، فنل فتالئین برای تیتراسیون اسید-باز، و محلول های نشاسته برای فرآیند ردوکس نوع یدومتری. با این حال، اندازهگیریهای هدایت الکتریکی نیز میتوانند به عنوان ابزاری برای تعیین نقطه پایانی مورد استفاده قرار گیرند، برای مثال هنگام مشاهده محلولی از HCl با پایه قوی NaOH.
خنثی سازی پروتون
با پیشرفت تیتراسیون، پروتون ها خنثی می شوند تا با تشکیل آب، NaOH را تشکیل دهند. به ازای هر مقدار NaOH اضافه شده، تعداد معادلی یون هیدروژن حذف می شود. در واقع، کاتیون H+ متحرک با یون Na+ کمتر متحرک جایگزین می شود و رسانایی محلول تیتر شده و همچنین هدایت سلولی اندازه گیری شده کاهش می یابد. این کار تا زمانی ادامه می یابد که به یک نقطه هم ارزی برسد که در آن محلولی از کلرید سدیم NaCl به دست آید. اگر باز بیشتری اضافه شود، با اضافه شدن یون های Na+ و OH- بیشتر افزایش می یابد و واکنش خنثی سازی دیگر مقدار قابل توجهی از H+ را حذف نمی کند.

در نتیجه، وقتی یک اسید قوی با یک باز قوی تیتر می شود، رسانایی در نقطه هم ارزی حداقل است. این حداقلمی توان به جای رنگ نشانگر برای تعیین نقطه پایانی تیتراسیون استفاده کرد. منحنی تیتراسیون نموداری از مقادیر اندازه گیری شده رسانایی یا رسانایی به عنوان تابعی از حجم محلول NaOH اضافه شده است. منحنی تیتراسیون را می توان برای تعیین نموداری نقطه هم ارزی استفاده کرد. روش هدایت سنجی آنالیز (و استفاده از آن) در شیمی مدرن بسیار مرتبط است.
واکنش
برای واکنش بین یک باز ضعیف اسیدی ضعیف، هدایت الکتریکی ابتدا تا حدودی کاهش می یابد، زیرا تعداد کمی از یون های H+ موجود استفاده می شود. سپس رسانایی به دلیل سهم کاتیون نمک و آنیون تا حجم نقطه هم ارزی کمی افزایش می یابد (این سهم در مورد یک باز اسیدی قوی ناچیز است و در آنجا در نظر گرفته نمی شود.) پس از رسیدن به نقطه هم ارزی رسانایی به دلیل یون های OH اضافی به سرعت افزایش می یابد.
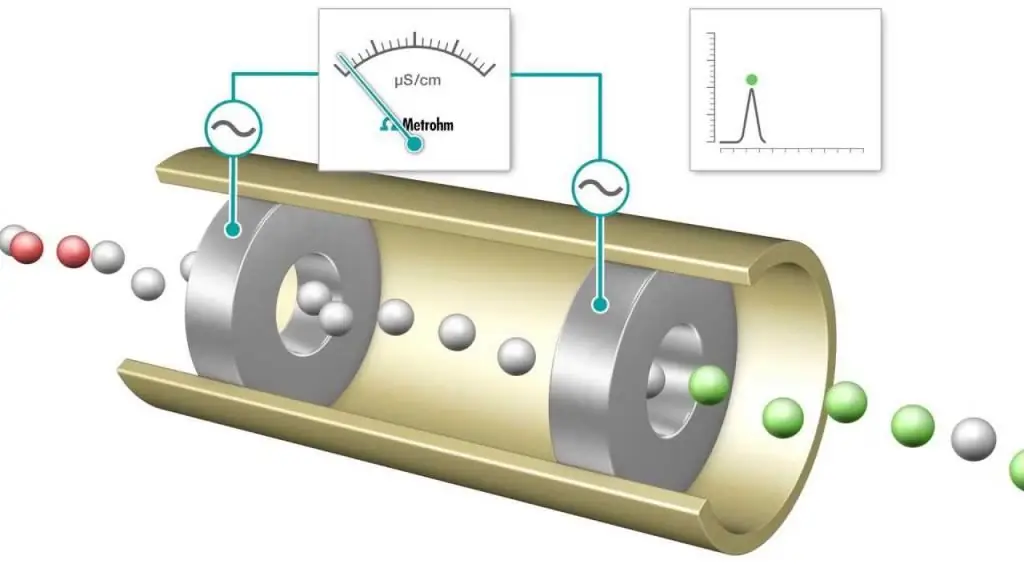
آشکارسازهای رسانایی (روش آنالیز هدایت سنجی) نیز برای اندازه گیری غلظت الکترولیت در محلول های آبی استفاده می شود. غلظت مولی آنالیت که رسانایی محلول را ایجاد می کند را می توان از مقاومت الکتریکی اندازه گیری شده محلول به دست آورد.
روش آنالیز هدایت سنجی: اصل و فرمول
(2.4.13) C=Constcell1Λm1Res، که در آن Constcell یک مقدار ثابت بسته به سلول اندازه گیری است، Res مقاومت الکتریکی اندازه گیری شده توسط دستگاه است (طبق قانون اهم Res=I / V، و با یک ثابت اندازه گیری ولتاژ V شدت I به شما امکان می دهد Res را محاسبه کنید، و Λm معادل آن استرسانایی برای ذرات یونی اگرچه برای اهداف عملی لm را می توان ثابت در نظر گرفت، اما طبق قانون کولراوش به غلظت بستگی دارد:
(2.4.14)=Ht Λm0-ΘC، که Θ یک ثابت است و Λm0 مشخصه رسانایی مولی محدود کننده هر یون است. رسانایی مولی به نوبه خود به دما بستگی دارد.
Scrit
توسعه روش هدایت سنجی تحلیل اندازه گیری، دانشمندان را به اکتشافات جدیدی سوق داده است. دانشمندان نسبت فوق اشباع بحرانی Scrit را با استفاده از رسانایی سنجی در یک سیستم بارشی همگن AgCl بیش از یون Ag+، با استفاده از هیدرولیز آلکیل کلرید به عنوان منبع یون CI تعیین کردند. آنها Scrit=1.51، 1.73 و 1.85 را به ترتیب در دمای 15، 25 و 35 درجه سانتیگراد یافتند که در آن S=([Ag+][Cl-] / Ksp) 1/2 بر اساس تعریف آنها بود. اگر این تعریف از ضریب فوق اشباع به تعریف ما تبدیل شود (S=[Ag+][Cl-] / Ksp)، نتایج به ترتیب 2.28، 2.99 و 3.42 هستند که مطابقت نسبتاً خوبی با نتایج مطالعه حاضر دارند. با این حال، وابستگی دمای Scrit برخلاف آنچه در مطالعه حاضر توضیح داده شده است. اگرچه دلیل این تناقض مشخص نیست، کاهش Scrit با افزایش دما ممکن است کاملاً معقول باشد، زیرا سرعت هستهزایی با یک تغییر کوچک در ΔGm/ kT به طور چشمگیری تغییر میکند و بنابراین ΔGm/ kT که متناسب با T است. - 3 (lnSm) 2 طبق فرمول (1.4.12) با تغییر دما در سیستم داده شده تقریباً ثابت در نظر گرفته می شود. در ضمن، تعریف S باید [Ag +] [Cl -] / Ksp باشد، زیرا نسبت فوق اشباع بر حسبغلظت مونومر [AgCl] در ابتدا به صورت S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp. داده می شود.
Tanaka و Iwasaki
تاریخچه روش تحلیل رسانایی توسط دو دانشمند برجسته ژاپنی ادامه یافت. تاناکا و ایوازاکی فرآیند هستهزایی ذرات AgCl و AgBr را با استفاده از روش جریان متوقف شده در ترکیب با یک اسپکتروفتومتر چند کانالی مورد مطالعه قرار دادند که برای مطالعه یک فرآیند سریع به ترتیب msec مفید است. آنها دریافتند که مقداری از مجتمع هالید نقره خاص AgXm (m-1)، با باند جذب نسبتاً باریک UV، بلافاصله هنگامی که محلولی از AgC104 از مرتبه 10-4 mol dm-3 با KX مخلوط شد، تشکیل شد (X=کلر یا Br) محلول از مرتبه 10-2 تا 10-1 mol dm-3 به دنبال فروپاشی سریع آن در حدود 10 ms با تشکیل یک محصول میانی با جذب گسترده UV و تغییر بسیار کندتر در طیف از محصول میانی آنها حد واسط را به عنوان هسته های تک پراکنده (AgX) n متشکل از n مولکول تفسیر کردند و n را از نسبت ظاهری -dC/dt α Cn در t=0 برای غلظت های اولیه مختلف از پیش ساز C AgXm (m-1) - (n=7) تعیین کردند. -10 برای AgCl، n=3-4 برای AgBr).

با این حال، از آنجایی که پیش ساز AgXm (m − 1) به روشی غیر ایستا تجزیه می شود، نظریه هسته زایی شبه ساکن در این فرآیند اعمال نمی شود، و بنابراین مقدار حاصل از n با nمقدار هسته های بحرانی. اگر محصول میانی حاوی هسته های تک پراکنده باشد،تشکیل شده توسط کمپلکس مونومر، نسبت αC -dC/dt ممکن است حفظ نشود. مگر اینکه فرض کنیم خوشه های کوچکتر از n-mers در تعادل هستند، ki - 1، ici - 1c1=ki، i - 1ci، با یکدیگر در یک واکنش متوالی c1 → c2 → c3 →… → cn − 1 → cn. و فقط آخرین مرحله cn − 1 → cn برگشت ناپذیر است. یعنی c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
علاوه بر این، باید فرض کرد که غلظت های خوشه ها از 2 تا n-1 دارای غلظت های ناچیز تعادلی هستند. با این حال، به نظر می رسد هیچ مبنایی برای توجیه این فرضیات وجود ندارد. از سوی دیگر، ما سعی کردیم شعاع هسته های بحرانی و ضرایب فوق اشباع S را در پایان فرآیند سریع محاسبه کنیم، با استفاده از γ=101 mJ m-2 برای AgCl19 مکعب و γ=109 mJ m-2 برای AgBr20 مکعبی، با فرض اینکه مقادیر n، 7-10 برای AgCl19 و 3-4 برای AgBr20، معادل اندازه هسته های تک پراکنده، n است. روش تجزیه و تحلیل هدایت سنجی، که بررسی های آن از تایید ساده تا تحسین را شامل می شود، تولد جدیدی برای شیمی به عنوان یک علم ایجاد کرد.
در نتیجه، دانشمندان فرمول زیر را کشف کردند: r=0.451 نانومتر و S=105 برای AgCl با n=9. r=0.358 نانومتر و S=1230 برای AgBr با n=4. از آنجایی که سیستم های آنها با سیستم های دیویس و جونز قابل مقایسه است، که یک فوق اشباع بحرانی AgCl در حدود 1.7-2.0 در دمای 25 درجه سانتیگراد به دست آوردند. با استفاده از رسانایی اختلاط مستقیم در حجم های مساوی از محلول های آبی رقیق AgNO3 و KCl، مقادیر بسیار بالای S ممکن است فاکتورهای فوق اشباع واقعی را منعکس نکند.در تعادل با هسته های میانی.
جذب UV
به نظر منطقی تر است که یک واسطه با جذب گسترده UV را به هسته های بسیار بزرگتر از متوسط با توزیع اندازه وسیع که توسط یک واکنش متوالی غیر ثابت ایجاد می شود نسبت دهیم. به نظر می رسد تغییر آهسته بعدی هسته های میانی مربوط به بلوغ آنها در استوالد باشد.

در زمینه فوق، شیمیدان آمریکایی نیلسن نیز یک n مشابه در حدود 12 و یک S مربوطه بزرگتر از 103 را برای هسته زایی ذرات سولفات باریم از اندازه گیری های کدورت به عنوان تابعی از فوق اشباع، با استفاده از n=dlogJ به دست آورد. / dlogC در یک نظریه بچر-درینگ مانند به فرمول. (1.3.37)، اما دادن (n+ 1) به جای n. از آنجایی که محلولهای یونهای باریم و یونهای سولفات مستقیماً در این آزمایش با هم مخلوط شدند، هستهزایی سریع گذرا باید بلافاصله پس از اختلاط به پایان میرسید، و آنچه اندازهگیری شد میتواند سرعت بلوغ آهسته استوالد و/یا همجوشی هستههای تولید شده باشد. ظاهراً دلیل کوچک بودن غیرمنطقی n و فوق اشباع فوق العاده بالای آن است. بنابراین، باید مجدداً توجه داشته باشیم که برخی از مخازن گونههای مونومر که در پاسخ به مصرف آنها را آزاد میکند، همیشه برای دستیابی به هستهزایی شبه ثابت در یک سیستم بسته ضروری است. تمام نظریه های کلاسیک هسته زایی، از جمله نظریه بچر-دورینگ، به طور ضمنی چنین شرطی را فرض می کنند. تعریف هدایت سنجیروش تجزیه و تحلیل در بخش های مقاله بالا ارائه شد.
دانشمندان دیگر فرآیند هستهزایی گذرا هالید نقره را با تجزیه رادیویی پالسی آب حاوی متیلن هالید و یونهای نقره بررسی کردهاند که در طی آن متیلن هالید برای آزاد کردن یونهای هالید توسط الکترونهای هیدراته تولید شده توسط تابش پالسی در محدوده تجزیه میشود. از 4 ns تا 3 میکرو ثانیه طیفهای محصولات با استفاده از یک مولتیپلایر و دوربین رگهای ثبت شد و پیشسازهای هالید نقره مونومری در طول زمان به ترتیب میکروثانیه تشکیل شدند و پس از آن فرآیند هستهزایی مشابه آنچه توسط تاناکا و ایوازاکی مشاهده شد، شکل گرفت. نتایج آنها به وضوح نشان می دهد که فرآیند هسته زایی هالیدهای نقره با اختلاط مستقیم واکنش دهنده ها شامل دو مرحله ابتدایی است. یعنی تشکیل یک پیش ساز مونومر از مرتبه μs و انتقال بعدی به هسته های مرتبه 10 میلی ثانیه. لازم به ذکر است که اندازه متوسط هسته ها حدود 10 نانومتر است.
اشباع
با توجه به ضرایب فوق اشباع برای هستهزایی ذرات AgCl در سیستمهای باز که در آن غلظتهای بالایی از واکنشدهندهها مانند AgNO3 و KCl به طور مداوم در طول بارندگی به محلول ژلاتین وارد میشوند، Strong و Wey31 1.029 (80 درجه سانتیگراد) گزارش کردند - 1.260 (40 درجه سانتیگراد) و Leubner32 1.024 در 60 درجه سانتیگراد را گزارش کردند که از اندازه گیری نرخ رشد ذرات دانه AgCl در حالت فوق اشباع بحرانی تخمین زده شد. این ماهیت روش هدایت سنجی تحلیل کمی است.
از سوی دیگر، برای سیستم های ذرات AgBr باز، برخی از آنهامقادیر تخمینی ضریب فوق اشباع بحرانی، Scrit: Scrit ~ 1.5 در 70 درجه سانتی گراد با توجه به Wey و Strong33 از حداکثر نرخ رشد وابسته به اندازه که با یافتن آستانه هستهزایی در نرخهای مختلف افزودن محلول AgNO3 به KBr تعیین میشود. محلول در حضور ذرات دانه توسط جت های دوگانه. Scrit=1.2-1.5 در دمای 25 درجه سانتیگراد طبق Jagannathan و Wey34 به عنوان حداکثر ضریب فوق اشباع تعیین شده از معادله گیبز-تامسون با داده های آنها در مورد حداقل میانگین اندازه هسته ها مشاهده شده توسط میکروسکوپ الکترونی در طول مرحله هسته زایی بارش AgBr دو جت.. این در هنگام اعمال روش کمی سنجی هدایت سنجی بسیار موثر است.

هنگام محاسبه این مقادیر Scrit، آنها γ=140 mJ m − 2 را گرفتند. از آنجایی که هستهزایی در سیستمهای باز مربوط به فرآیند بقای هستههای نوپا ایجاد شده در ناحیه محلی با فوق اشباع بسیار بالا در نزدیکی خروجیهای واکنش دهنده است، بسیار مهم است. اگر از داده های Sugimoto35 در مورد حداکثر شعاع هسته های AgBr در سیستم های باز (3.3 8.3 نانومتر) با γ نظری برای AgBr مکعبی (=109 mJ m-2) استفاده کنیم، فوق اشباع مربوط به غلظت املاح در تعادل با هسته های حداکثر اندازه است.) 3، سپس ضریب فوق اشباع بحرانی، Scrit، به اندازه 1.36 در 25 درجه سانتیگراد محاسبه می شود (اگر γ 140 mJ/m2 فرض شود، Scrit=1.48).
در نتیجه، در هر صورت، فوق اشباع بحرانی درسیستم های باز ذرات هالید نقره معمولاً بسیار کمتر از حداکثر فوق اشباع (احتمالاً نزدیک به فوق اشباع بحرانی) در سیستم های بسته هستند. دلیل این امر این است که شعاع متوسط هسته های تولید شده در ناحیه محلی یک سیستم باز بسیار بزرگتر از rmدر یک سیستم بسته است که احتمالاً به دلیل همجوشی آنی هسته های اولیه بسیار متمرکز در ناحیه محلی یک سیستم باز با یک سیستم باز بالا است. غلظت الکترولیت موضعی.
برنامه
استفاده از روش تیتراسیون هدایت سنجی برای ثبت پیوسته در طول فرآیندهای آنزیمی به طور گسترده مورد مطالعه و تجزیه و تحلیل قرار گرفته است. تقریباً تمام روشهای تحلیلی الکتروشیمیایی مبتنی بر واکنشهای الکتروشیمیایی (پتانسیومتری، ولتامتری، آمپرومتری، کولومتری) هستند.
روش آنالیز هدایت سنجی روشی است که در آن یا اصلاً واکنش های الکتروشیمیایی روی الکترودها وجود ندارد یا واکنش های ثانویه ای وجود دارد که می توان از آنها چشم پوشی کرد. بنابراین در این روش مهمترین خاصیت محلول الکترولیت در لایه مرزی رسانایی الکتریکی آن است که با توجه به طیف نسبتاً وسیعی از واکنش های بیولوژیکی متفاوت است.
مزایا
حسگرهای زیستی رسانایی سنجی نسبت به انواع دیگر مبدل ها نیز مزایایی دارند. اول، آنها را می توان با استفاده از تکنولوژی استاندارد لایه نازک کم هزینه ساخت. این امر، همراه با استفاده از روشی بهینه برای بی حرکت کردن مواد بیولوژیکی، منجر به کاهش قابل توجهی در هزینه اولیه دستگاه ها وهزینه کل تجزیه و تحلیل برای میکروبیوسنسورهای داخلی، اجرای حالت اندازهگیری دیفرانسیل آسان است که تأثیرات خارجی را جبران میکند و دقت اندازهگیری را تا حد زیادی بهبود میبخشد.
داده ها به وضوح پتانسیل بالای بیوسنسورهای هدایت سنجی را نشان می دهند. با این حال، این هنوز یک روند نسبتاً جدید در حسگرهای زیستی است، بنابراین توسعه دستگاه های تجاری آینده امیدوارکننده ای دارد.
روش های جدید
برخی از دانشمندان یک روش کلی برای اندازه گیری pKa با رسانایی توصیف کرده اند. این روش تا حدود سال 1932 (قبل از استفاده از روش های اندازه گیری pH) به طور گسترده مورد استفاده قرار می گرفت. روش هدایت سنجی بسیار حساس به دما است و نمی توان از آن برای اندازه گیری مقادیر همپوشانی pKa استفاده کرد. یک مزیت احتمالی برای نمونههای بدون کروموفور این است که میتوان آن را در محلولهای بسیار رقیق، کمتر از 2.8 × 10-5 M استفاده کرد. در سالهای اخیر، هدایت سنجی 87 برای اندازهگیری pKa لیدوکائین استفاده شده است، اگرچه نتیجه بهدستآمده 0.7 بود. در هر واحد کمتر از مقدار pH عمومی پذیرفته شده.

آلبرت و سرجنت همچنین روشی را برای تعیین pKa از اندازهگیریهای حلالیت توصیف کردند. همانطور که در بالا ذکر شد، حلالیت به pKa وابسته است، بنابراین اگر حلالیت در مقادیر pH متعدد در یک منحنی اندازهگیری شود، pKa میتواند تعیین شود. پک و بنت یک روش کلی برای تخمین مقادیر pKa برای مواد تکپروتیک، دوپروتیک و آمفوتریک با مجموعهای از اندازهگیریهای حلالیت و pH توصیف کردند. هانسن و هافلیگر pKa نمونه را به دست آوردند کهبه سرعت با هیدرولیز از سرعت انحلال اولیه خود به عنوان تابعی از pH در یک دستگاه دیسک چرخان تجزیه می شود. نتیجه به خوبی با نتیجه pH/UV مطابقت دارد، اما تجزیه روش دوم را دشوار می کند. این به طور کلی توصیفی از روش هدایت سنجی تحلیل است.






