ترمودینامیک حالت مجموع گازی ماده شاخه مهمی از فیزیک است که تعادل ترمودینامیکی و انتقال شبه استاتیکی در سیستم ها را مطالعه می کند. مدل اصلی که پیش بینی رفتار سیستم ها بر اساس آن است، مدل گاز ایده آل است. با استفاده از آن معادله مندلیف-کلاپیرون به دست آمد. آن را در مقاله در نظر بگیرید.
گاز ایده آل
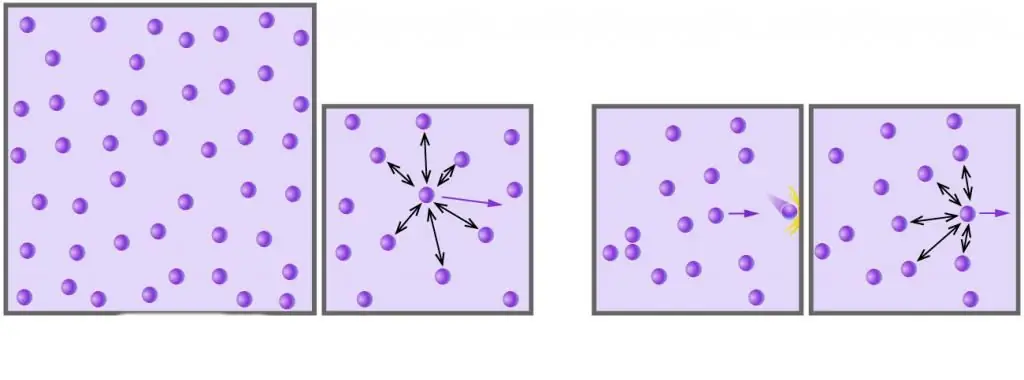
همانطور که می دانید، همه گازهای واقعی از مولکول ها یا اتم هایی تشکیل شده اند که فاصله بین آنها در مقایسه با اندازه آنها در فشارهای پایین بسیار زیاد است. علاوه بر این، در دماهای بالا، در مقیاس مطلق، انرژی جنبشی مولکولها از انرژی پتانسیل مرتبط با برهمکنشهای ضعیف دوقطبی-دوقطبی تجاوز میکند (اگر علاوه بر این برهمکنشها، انواع دیگری از پیوندهای شیمیایی، به عنوان مثال، یونی یا هیدروژن، سپس آنها سهم قابل توجهی در جزء بالقوه انرژی سیستم داخلی دارند).
به دلیلبرای بسیاری از گازهای واقعی در شرایط نزدیک به نرمال، می توان از تعاملات داخلی و اندازه ذرات آنها غافل شد. این دو تقریب اصلی مدل گاز ایده آل را تشکیل می دهند.
معادله مندلیف در فیزیک

صحیح تر و منصفانه تر است که این معادله را قانون کلاپیرون- مندلیف بنامیم. واقعیت این است که اولین بار توسط مهندس فرانسوی امیل کلاپیرون در سال 1834 ثبت شد. او این کار را با تجزیه و تحلیل قوانین گاز بویل-ماریوت، گی-لوساک و چارلز در آغاز قرن نوزدهم انجام داد.
شایستگی دیمیتری مندلیف شیمیدان روسی در این واقعیت نهفته است که او به معادله یک شکل ریاضی مدرن و آسان برای استفاده داد. به طور خاص، مندلیف یک ثابت برای همه گازها R=8، 314 J/(molK) وارد معادله کرد. کلاپیرون خود از تعدادی ثابت تجربی استفاده کرد که فرآیند محاسباتی را دشوار می کند.
معادله مندلیف-کلاپیرون به صورت زیر نوشته می شود:
PV=nRT.
این برابری به این معنی است که حاصل ضرب فشار P و حجم V در سمت چپ عبارت همیشه با حاصلضرب دمای مطلق T و مقدار ماده n در سمت چپ متناسب است.
عبارت مورد مطالعه به شما این امکان را می دهد که هر قانون گاز را اگر دو پارامتر از چهار پارامتر آن را اصلاح کنید، به دست آورید. در مورد ایزوفرایندها، سیستم های بسته ای مورد مطالعه قرار می گیرند که در آنها تبادل ماده با محیط وجود ندارد (n=const). این فرآیندها با یک پارامتر ترمودینامیکی ثابت (T، P یا V) مشخص می شوند.

مشکل مثال
حالا بیایید مسئله معادله مندلیف-کلاپیرون را حل کنیم. مشخص است که اکسیژن به وزن 500 گرم در یک سیلندر با حجم 100 لیتر در فشار 2 اتمسفر است. با توجه به اینکه سیستم در تعادل ترمودینامیکی است، دمای بالون چقدر است.
به یاد بیاورید که طبق تعریف، مقدار یک ماده با فرمول محاسبه می شود:
n=m/M.
جایی که m جرم همه ذرات سیستم است، M جرم مولی متوسط آنهاست. این برابری به ما امکان می دهد معادله مندلیف را به شکل زیر بازنویسی کنیم:
PV=mRT/M.
از کجا فرمول کار برای این کار را دریافت می کنیم:
T=PVM/(mR).
باقی می ماند که همه کمیت ها را به واحدهای SI تبدیل کنیم و آنها را به این عبارت جایگزین کنیم:
T=21013250، 10، 032/(0، 58، 314)=156 K.
دمای محاسبه شده -117 oC است. اگرچه اکسیژن در این دما هنوز گازی است (در 182.96 oC متراکم می شود)، در چنین شرایطی مدل گاز ایده آل را فقط می توان برای به دست آوردن یک تخمین کیفی از مقدار محاسبه شده استفاده کرد.






