در ترمودینامیک، هنگام مطالعه انتقال از حالت اولیه به نهایی یک سیستم، دانستن اثر حرارتی فرآیند بسیار مهم است. مفهوم ظرفیت گرمایی ارتباط نزدیکی با این اثر دارد. در این مقاله، این سوال را بررسی خواهیم کرد که منظور از ظرفیت گرمایی ایزوکوریک یک گاز چیست.
گاز ایده آل
گاز ایده آل گازی است که ذرات آن به عنوان نقاط مادی در نظر گرفته می شوند، یعنی دارای ابعاد نیستند، بلکه جرم دارند و در آن تمام انرژی درونی صرفاً از انرژی جنبشی حرکت مولکول ها تشکیل شده است. و اتم ها.
هر گاز واقعی در حالت ایده آل هرگز مدل توصیف شده را برآورده نمی کند، زیرا ذرات آن هنوز برخی از ابعاد خطی دارند و با استفاده از پیوندهای ضعیف واندروالس یا پیوندهای شیمیایی از نوع دیگر با یکدیگر تعامل دارند. با این حال، در فشارهای پایین و دماهای بالا، فواصل بین مولکول ها زیاد است و انرژی جنبشی آنها ده ها برابر از انرژی پتانسیل بیشتر می شود. همه اینها امکان اعمال مدل ایده آل برای گازهای واقعی را با درجه بالایی از دقت ممکن می سازد.
انرژی داخلی گاز
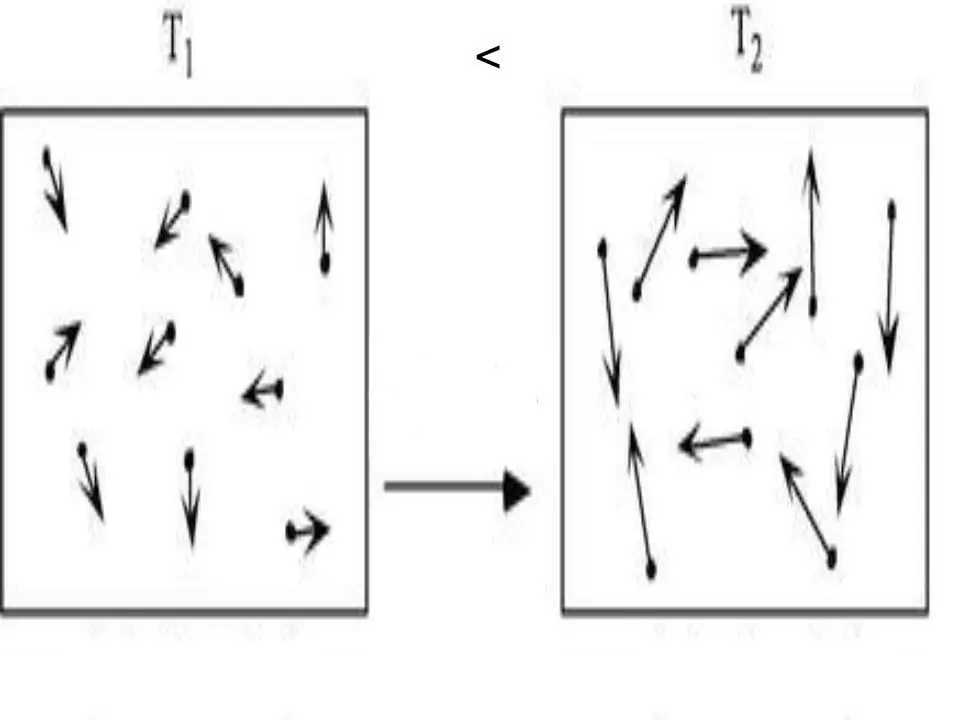
انرژی درونی هر سیستم یک ویژگی فیزیکی است که برابر است با مجموع انرژی پتانسیل و جنبشی. از آنجایی که انرژی پتانسیل را می توان در گازهای ایده آل نادیده گرفت، می توانیم برابری را برای آنها بنویسیم:
U=Ek.
که در آن Ek انرژی سیستم جنبشی است. با استفاده از نظریه جنبشی مولکولی و به کارگیری معادله حالت کلی کلاپیرون- مندلیف، به دست آوردن یک عبارت برای U دشوار نیست. در زیر نوشته شده است:
U=z/2nRT.
در اینجا T، R و n به ترتیب دمای مطلق، ثابت گاز و مقدار ماده هستند. مقدار z یک عدد صحیح است که تعداد درجات آزادی یک مولکول گاز را نشان می دهد.
ظرفیت حرارتی ایزوباریک و ایزوکوریک
در فیزیک، ظرفیت گرمایی مقدار گرمایی است که باید به سیستم مورد مطالعه داده شود تا یک کلوین گرم شود. تعریف معکوس نیز صادق است، یعنی ظرفیت گرمایی مقدار گرمایی است که سیستم با سرد شدن یک کلوین آزاد می کند.
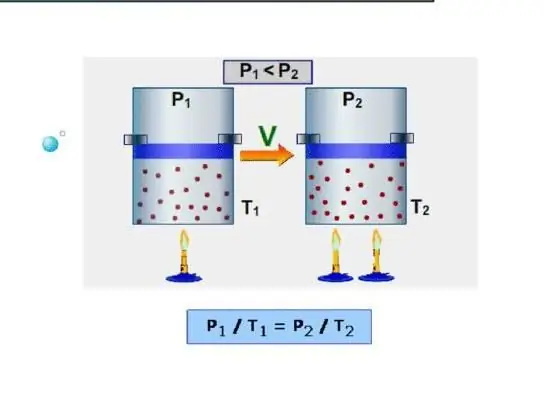
ساده ترین راه برای یک سیستم تعیین ظرفیت گرمایی ایزوکوریک است. به عنوان ظرفیت گرمایی در حجم ثابت درک می شود. از آنجایی که سیستم در چنین شرایطی کار نمی کند، تمام انرژی صرف افزایش ذخایر انرژی داخلی می شود. اجازه دهید ظرفیت گرمایی ایزوکوریک را با نماد CV نشان دهیم، سپس می توانیم بنویسیم:
dU=CVdT.
یعنی تغییر انرژی درونیاین سیستم با تغییر دمای آن نسبت مستقیم دارد. اگر این عبارت را با برابری نوشته شده در پاراگراف قبل مقایسه کنیم، به فرمول CV در گاز ایده آل می رسیم:
СV=z/2nR.
این مقدار برای استفاده در عمل ناخوشایند است، زیرا به مقدار ماده در سیستم بستگی دارد. بنابراین، مفهوم ظرفیت گرمایی ایزوکوریک خاص معرفی شد، یعنی مقداری که یا به ازای هر 1 مول گاز یا به ازای هر 1 کیلوگرم محاسبه می شود. اجازه دهید اولین مقدار را با نماد CV نشان دهیم، دومی - با نماد CV. m. برای آنها می توانید فرمول های زیر را بنویسید:
CV=z/2R;
CVm=z/2R/M.
اینجا M جرم مولی است.
ایزوباریک ظرفیت گرمایی در عین حفظ فشار ثابت در سیستم است. نمونه ای از چنین فرآیندی انبساط گاز در سیلندر زیر پیستون هنگام گرم شدن است. برخلاف فرآیند ایزوکوریک، در طی فرآیند ایزوباریک، گرمای وارد شده به سیستم برای افزایش انرژی داخلی و انجام کارهای مکانیکی صرف می شود، یعنی:
H=dU + PdV.
آنتالپی یک فرآیند ایزوباریک حاصلضرب ظرفیت گرمایی ایزوباریک و تغییر دما در سیستم است، یعنی:
H=CPdT.
اگر انبساط را در فشار ثابت 1 مول گاز در نظر بگیریم، قانون اول ترمودینامیک به صورت زیر نوشته می شود:
CPdT=CV dT + RdT.
آخرین جمله از معادله به دست می آیدکلاپیرون- مندلیف. از این برابری رابطه بین ظرفیت گرمایی ایزوباریک و ایزوکوریک به دست می آید:
CP=CV + R.
برای یک گاز ایده آل، ظرفیت گرمایی مولی ویژه در فشار ثابت همیشه بیشتر از مشخصه ایزوکوریک مربوطه با R=8، 314 J/(molK) است.
درجات آزادی مولکول ها و ظرفیت گرمایی
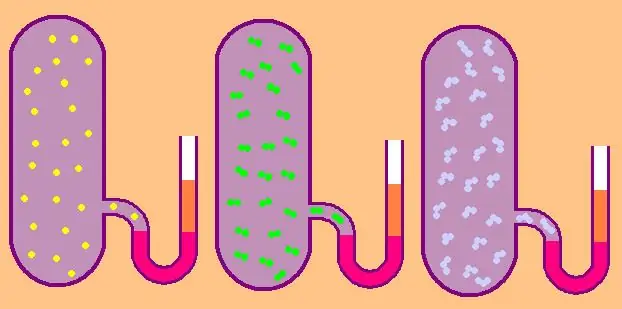
بیایید دوباره فرمول ظرفیت گرمایی ایزوکوریک مولی خاص را بنویسیم:
CV=z/2R.
در مورد گاز تک اتمی، مقدار z=3، زیرا اتمهای موجود در فضا فقط میتوانند در سه جهت مستقل حرکت کنند.
اگر در مورد گازی صحبت می کنیم که از مولکول های دو اتمی تشکیل شده است، به عنوان مثال، اکسیژن O2 یا هیدروژن H2، پس، علاوه بر حرکت انتقالی، این مولکول ها همچنان می توانند حول دو محور متقابل عمود بر هم بچرخند، یعنی z برابر با 5 خواهد بود.
برای مولکول های پیچیده تر، از z=6 استفاده کنید. برای تعیین CV






