بخش مهمی از ترمودینامیک مطالعه تحولات بین فازهای مختلف یک ماده است، زیرا این فرآیندها در عمل رخ می دهند و برای پیش بینی رفتار یک سیستم در شرایط خاص اهمیت اساسی دارند. به این تبدیل ها انتقال فاز می گویند که مقاله به آن اختصاص دارد.
مفهوم فاز و جزء سیستم

قبل از پرداختن به تغییر فاز در فیزیک، لازم است مفهوم خود فاز را تعریف کنیم. همانطور که از درس فیزیک عمومی مشخص است، ماده سه حالت دارد: گاز، جامد و مایع. در بخش خاصی از علم - در ترمودینامیک - قوانین برای مراحل ماده تنظیم می شوند، نه برای حالت های تجمع آنها. فاز به عنوان حجم معینی از ماده شناخته می شود که ساختاری همگن دارد، با خواص فیزیکی و شیمیایی خاص مشخص می شود و با مرزهایی از بقیه ماده جدا می شود که به آن فاز بین فاز می گویند.
بنابراین، مفهوم "فاز" حاوی اطلاعات عملی بسیار مهم تری در مورد خواص است.ماده از حالت تجمع آن. به عنوان مثال، حالت جامد فلزی مانند آهن میتواند در مراحل زیر باشد: مکعب مغناطیسی در مرکز بدنه با دمای پایین (BCC)، bcc غیر مغناطیسی دمای پایین، مکعب محور (fcc) و بالا دمای غیر مغناطیسی bcc.
علاوه بر مفهوم "فاز"، قوانین ترمودینامیک از اصطلاح "مؤلفه ها" نیز استفاده می کند که به معنای تعداد عناصر شیمیایی تشکیل دهنده یک سیستم خاص است. این بدان معنی است که فاز می تواند تک جزئی (1 عنصر شیمیایی) یا چند جزئی (چند عنصر شیمیایی) باشد.
قضیه گیبس و تعادل بین فازهای سیستم

برای درک انتقال فازها، دانستن شرایط تعادل بین آنها ضروری است. این شرایط را می توان با حل سیستم معادلات گیبس برای هر یک از آنها از نظر ریاضی به دست آورد، با این فرض که حالت تعادل زمانی حاصل می شود که کل انرژی گیبس سیستم جدا شده از تأثیر خارجی دیگر تغییر نکند.
در نتیجه حل سیستم معادلات نشان داده شده، شرایطی برای وجود تعادل بین چند فاز به دست می آید: یک سیستم ایزوله تنها زمانی تکامل نمی یابد که فشارها، پتانسیل های شیمیایی هر جزء و دما در همه فازها. با هم برابرند.
قانون فاز گیبس برای تعادل

یک سیستم متشکل از چندین فاز و جزء می تواند نه تنها در تعادل باشد.تحت شرایط خاص، به عنوان مثال، در یک دما و فشار خاص. برخی از متغیرهای قضیه گیبس برای تعادل را می توان با حفظ تعداد فازها و تعداد اجزایی که در این تعادل هستند تغییر داد. تعداد متغیرهایی را که می توان بدون برهم زدن تعادل در سیستم تغییر داد، تعداد آزادی های این سیستم نامیده می شود.
تعداد آزادی های l یک سیستم متشکل از فازهای f و k اجزا به طور منحصر به فردی از قانون فاز گیبس تعیین می شود. این قانون از نظر ریاضی به صورت زیر نوشته می شود: l + f=k + 2. چگونه با این قانون کار کنیم؟ بسیار ساده. برای مثال مشخص است که سیستم از f=3 فاز تعادلی تشکیل شده است. حداقل تعداد اجزایی که چنین سیستمی می تواند داشته باشد چقدر است؟ شما میتوانید با استدلال به این سؤال پاسخ دهید: در مورد تعادل، سختترین شرایط زمانی وجود دارد که فقط در شاخصهای خاصی تحقق یابد، یعنی تغییر در هر پارامتر ترمودینامیکی منجر به عدم تعادل میشود. این بدان معناست که تعداد آزادی ها l=0 است. با جایگزینی مقادیر شناخته شده l و f، k=1 را بدست می آوریم، یعنی سیستمی که در آن سه فاز در تعادل هستند می تواند از یک جزء تشکیل شده باشد. یک مثال بارز نقطه سه گانه آب است که در آن یخ، آب مایع و بخار در دماها و فشارهای خاص در حالت تعادل هستند.
طبقهبندی تبدیلهای فاز
اگر شروع به تغییر برخی از پارامترهای ترمودینامیکی در یک سیستم در حالت تعادل کنید، می توانید مشاهده کنید که چگونه یک فاز ناپدید می شود و فاز دیگری ظاهر می شود. یک مثال ساده از این فرآیند، ذوب شدن یخ هنگام گرم شدن است.
با توجه به اینکه معادله گیبس فقط به دو متغیر (فشار و دما) بستگی دارد و انتقال فاز شامل تغییر در این متغیرها است، بنابراین از نظر ریاضی انتقال بین فازها را می توان با تمایز انرژی گیبس با توجه به آن توصیف کرد. متغیرها این رویکردی بود که توسط فیزیکدان اتریشی پل ارنفست در سال 1933 استفاده شد، زمانی که او طبقه بندی تمام فرآیندهای ترمودینامیکی شناخته شده ای را که با تغییر در تعادل فاز رخ می دهند جمع آوری کرد.
از مبانی ترمودینامیک چنین برمی آید که اولین مشتق انرژی گیبس نسبت به دما برابر با تغییر آنتروپی سیستم است. مشتق انرژی گیبس نسبت به فشار برابر با تغییر حجم است. اگر، زمانی که فازهای سیستم تغییر می کنند، آنتروپی یا حجم دچار شکستگی می شود، یعنی به طور ناگهانی تغییر می کنند، آنگاه از انتقال فاز مرتبه اول صحبت می کنند.
بعلاوه، دومین مشتقات انرژی گیبس با توجه به دما و فشار به ترتیب ظرفیت گرمایی و ضریب انبساط حجمی هستند. اگر تبدیل بین فازها با ناپیوستگی در مقادیر کمیت های فیزیکی مشخص شده همراه باشد، آنگاه از انتقال فاز مرتبه دوم صحبت می شود.
نمونه هایی از تبدیل بین فازها

تعداد زیادی انتقال مختلف در طبیعت وجود دارد. در چارچوب این طبقهبندی، نمونههای بارز انتقال از نوع اول، فرآیندهای ذوب فلزات یا تراکم بخار آب از هوا، هنگامی که یک جهش حجمی در سیستم وجود دارد، است.
اگر در مورد انتقال های مرتبه دوم صحبت کنیم، نمونه های بارز تبدیل آهن از حالت مغناطیسی به حالت پارامغناطیس در یک دما است.768 درجه سانتیگراد یا تبدیل یک رسانای فلزی به حالت ابررسانا در دمای نزدیک به صفر مطلق.
معادلاتی که انتقال های نوع اول را توصیف می کنند
در عمل، اغلب لازم است بدانیم که چگونه دما، فشار و انرژی جذب شده (آزاد شده) در یک سیستم زمانی که تبدیل فاز در آن رخ می دهد، تغییر می کند. برای این منظور از دو معادله مهم استفاده می شود. آنها بر اساس دانش مبانی ترمودینامیک به دست آمده اند:
فرمول
فرمول
استفاده از هر دو معادله نه تنها در به دست آوردن وابستگی های کمی کمیت های فیزیکی، بلکه در تعیین علامت شیب منحنی های تعادل در نمودارهای فازی نیز می باشد.
معادله برای توصیف انتقال های نوع دوم

انتقال فاز از نوع 1 و 2 با معادلات مختلف توصیف می شود، زیرا استفاده از معادلات کلازیوس و کلازیوس برای انتقال های مرتبه دوم منجر به عدم قطعیت ریاضی می شود.
برای توصیف دومی، از معادلات Ehrenfest استفاده می شود که رابطه ای بین تغییرات فشار و دما از طریق آگاهی از تغییرات ظرفیت گرمایی و ضریب انبساط حجمی در طول فرآیند تبدیل ایجاد می کند. معادلات ارنفست برای توصیف انتقال هادی-ابررسانا در غیاب میدان مغناطیسی استفاده می شود.
اهمیتنمودارهای فاز
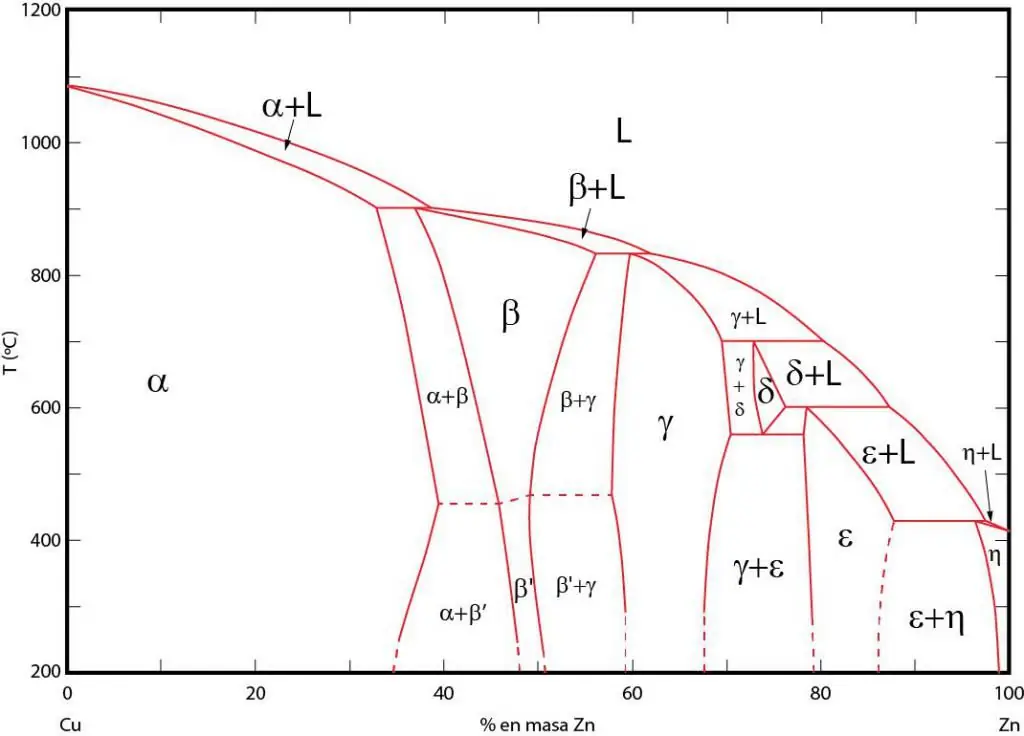
نمودارهای فاز، نمایشی گرافیکی از مناطقی هستند که در آن فازهای مربوطه در تعادل هستند. این مناطق با خطوط تعادل بین فازها از هم جدا می شوند. نمودارهای فاز P-T (فشار-دما)، T-V (دما-حجم)، و P-V (فشار-حجم) نمودارهای فاز اغلب استفاده می شود.
اهمیت نمودارهای فاز در این واقعیت نهفته است که آنها به شما امکان می دهند پیش بینی کنید که وقتی شرایط خارجی مطابق با آن تغییر کند، سیستم در چه فازی قرار می گیرد. این اطلاعات در عملیات حرارتی مواد مختلف به منظور به دست آوردن ساختاری با خواص مطلوب استفاده می شود.






