یکی از سؤالات مهم در مطالعه سیستم های ترمودینامیکی در فیزیک این سؤال است که آیا این سیستم می تواند کارهای مفیدی انجام دهد؟ مفهوم انرژی درونی ارتباط نزدیکی با مفهوم کار دارد. در این مقاله به بررسی انرژی داخلی گاز ایده آل می پردازیم و فرمول هایی برای محاسبه آن ارائه می کنیم.
گاز ایده آل
درباره گاز به عنوان حالت تجمعی که تحت تأثیر خارجی بر روی آن هیچ نیروی کشسانی ندارد و در نتیجه حجم و شکل خود را حفظ نمی کند، هر دانش آموز مدرسه ای می داند. مفهوم گاز ایده آل برای بسیاری نامفهوم و نامشخص است. بیایید آن را توضیح دهیم.
گاز ایده آل هر گازی است که دو شرط مهم زیر را برآورده کند:
- ذراتی که آن را تشکیل می دهند اندازه ندارند. آنها یک اندازه دارند، اما در مقایسه با فواصل بین آنها آنقدر کوچک است که می توان آن را در تمام محاسبات ریاضی نادیده گرفت.
- ذرات با استفاده از نیروها یا نیروهای واندروالسی با یکدیگر برهمکنش ندارندطبیعت دیگر در واقع، در همه گازهای واقعی، چنین برهمکنشی وجود دارد، اما انرژی آن در مقایسه با انرژی متوسط ذرات جنبشی ناچیز است.
شرایط توصیف شده تقریباً توسط همه گازهای واقعی که دمای آنها بالای 300 کلوین است و فشارها از یک اتمسفر تجاوز نمی کند، برآورده می شود. برای فشارهای خیلی بالا و دمای پایین انحراف گازها از رفتار ایده آل مشاهده می شود. در این مورد، از گازهای واقعی صحبت می شود. آنها با معادله واندروالس توصیف می شوند.
مفهوم انرژی داخلی یک گاز ایده آل
طبق تعریف، انرژی درونی یک سیستم، مجموع انرژی های جنبشی و پتانسیل موجود در این سیستم است. اگر این مفهوم برای یک گاز ایده آل اعمال شود، آنگاه جزء بالقوه باید دور ریخته شود. در واقع، از آنجایی که ذرات یک گاز ایدهآل با یکدیگر برهمکنش ندارند، میتوان آنها را آزادانه در خلاء مطلق حرکت کرد. برای استخراج یک ذره از سیستم مورد مطالعه، نیازی به انجام کار علیه نیروهای داخلی برهمکنش نیست، زیرا این نیروها وجود ندارند.
بنابراین، انرژی داخلی یک گاز ایده آل همیشه با انرژی جنبشی آن منطبق است. دومی، به نوبه خود، به طور منحصر به فرد توسط جرم مولی ذرات سیستم، تعداد آنها و همچنین میانگین سرعت حرکت انتقالی و چرخشی تعیین می شود. سرعت حرکت بستگی به دما دارد. افزایش دما منجر به افزایش انرژی داخلی می شود و بالعکس.
فرمول برایانرژی داخلی
انرژی داخلی یک سیستم گازی ایده آل را با حرف U نشان دهید. طبق ترمودینامیک، به عنوان تفاوت بین آنتالپی H سیستم و حاصلضرب فشار و حجم تعریف می شود، یعنی:.
U=H - pV.
در پاراگراف بالا، متوجه شدیم که مقدار U با کل انرژی جنبشی Ekهمه ذرات گاز مطابقت دارد:
U=Ek.
از مکانیک آماری، در چارچوب نظریه جنبشی مولکولی (MKT) یک گاز ایده آل، چنین بر می آید که میانگین انرژی جنبشی یک ذره Ek1 برابر است با مقدار زیر:
Ek1=z/2kBT.
در اینجا kB و T - ثابت و دما بولتزمن، z - تعداد درجات آزادی. کل انرژی جنبشی سیستم Ek را می توان با ضرب Ek1 در تعداد ذرات N در سیستم به دست آورد:
Ek=NEk1=z/2NkBT.
بنابراین، ما فرمول انرژی داخلی یک گاز ایده آل را به دست آورده ایم که به صورت کلی بر حسب دمای مطلق و تعداد ذرات در یک سیستم بسته نوشته شده است:
U=z/2NkBT.
گاز تک اتمی و چند اتمی
فرمول U نوشته شده در پاراگراف قبلی مقاله برای استفاده عملی آن ناخوشایند است، زیرا تعیین تعداد ذرات N دشوار است. با این حال، اگر تعریف مقدار ماده n را در نظر بگیریم، این عبارت را می توان به شکل راحت تری بازنویسی کرد:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
تعداد درجات آزادی z به هندسه ذرات سازنده گاز بستگی دارد. بنابراین، برای یک گاز تک اتمی، z=3، زیرا یک اتم می تواند به طور مستقل تنها در سه جهت از فضا حرکت کند. اگر گاز دو اتمی باشد، z=5 است، زیرا دو درجه آزادی چرخشی دیگر به سه درجه آزادی انتقالی اضافه می شود. در نهایت، برای هر گاز چند اتمی دیگر، z=6 (3 درجه آزادی انتقالی و 3 درجه آزادی دورانی). با در نظر گرفتن این موضوع، می توانیم فرمول های انرژی داخلی یک گاز ایده آل تک اتمی، دو اتمی و چند اتمی را به شکل زیر بنویسیم:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
نمونه ای از کار برای تعیین انرژی درونی
یک سیلندر 100 لیتری حاوی هیدروژن خالص در فشار 3 اتمسفر است. با فرض اینکه هیدروژن یک گاز ایده آل در شرایط معین است، باید تعیین کرد که انرژی داخلی آن چیست.

فرمول های فوق برای U حاوی مقدار ماده و دمای گاز است. در شرایط مشکل، مطلقاً چیزی در مورد این مقادیر گفته نشده است. برای حل مسئله، لازم است معادله کلی کلاپیرون- مندلیف را یادآوری کنیم. ظاهری دارد که در شکل نشان داده شده است.
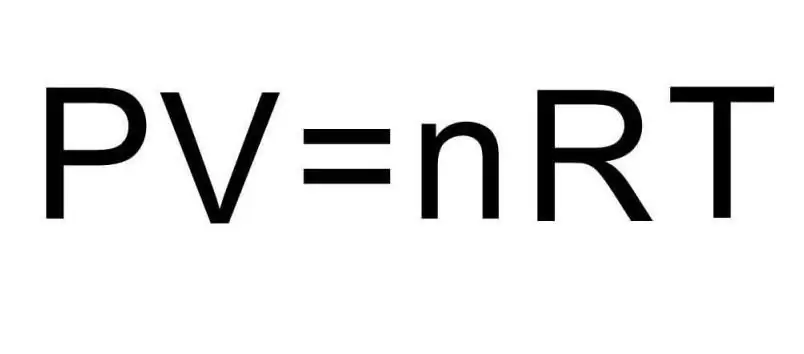
از آنجایی که هیدروژن H2 یک مولکول دو اتمی است، فرمول انرژی داخلی این است:
UH2=5/2nRT.
با مقایسه هر دو عبارت، به فرمول نهایی برای حل مسئله می رسیم:
UH2=5/2PV.
باقی مانده است که واحدهای فشار و حجم را از حالت به سیستم واحدهای SI تبدیل کنید، مقادیر مربوطه را در فرمول برای UH2 جایگزین کنید و مقدار را بدست آورید. پاسخ: UH2 ≈ 76 کیلوژول.






